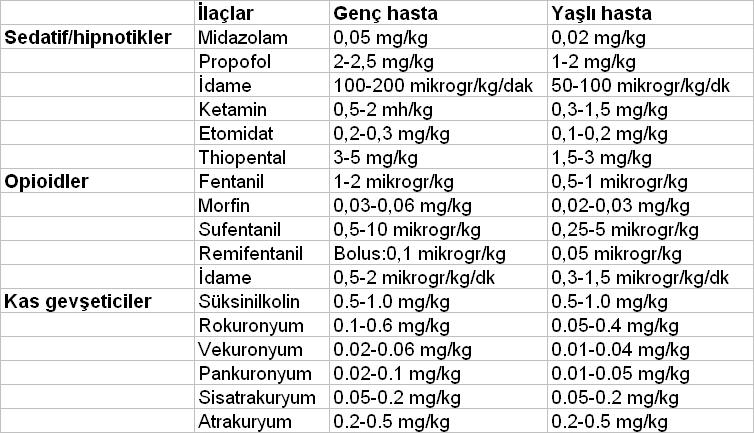
Bu yazıda geriatrik vakalarda kullanılan anestezik dozlarına değinilmektedir.
Volatil anestezikler:
İnhalasyon anesteziği ihtiyacı çoğu zaman ağrıya karşı oluşan hareketi tanımlayan MAK (minimum alveolar konsantrasyon) ile tarif edilir. Ancak şuursuzluk gibi diğer son noktalarda anestezinin oluşumu için gereklidir. MAKuyanık şuursuzluk (yani hastanın verilen emirleri yerine getirmemesi) için gerekli inhalasyon anestezik miktarının belirlemek için kullanılır; modern anestetikler için 0.33 MAK civarındadır. Hem MAK, hem de MAKuyanık yaşla azalır ve azalma miktarları birbirine benzer. 40 yaşın üzerindeki her yıl, MAK miktarında %0.6’lık bir azalma meydana gelir.
Bu azalmanın sebepleri pek açık olmamakla birlikte genel olarak yaşın – ister değişmiş sinaptik fonksiyon (presinaptik), ister değişmiş nöronal fonksiyon (postsinaptik) olsun- santral sinir sistemini etkilemesi ile açıklanabilir. Örneğin dopaminerjik ve kolinerjik nörotransmitter sistemler yaşlanma sırasında değişime uğrar; serbest radikal oluşumu yaşa bağımlıdır. Bunun dışında yaşla birlikte serebral atrofi, vasküler değişiklikler ve plaklar da meydana gelir. Ayrıca, inhalasyon anesteziği verilmesini takiben meydana gelen hareketsizlik spinal kord üzerinden yönetildiğinden, MAK’da meydana gelen değişimin bir parçasının da spinal korddan kaynaklandığı düşünülebilir.
Yaşlı hastalar ayrıca tiopental, propofol ve midazolam gibi intravenöz anestezik ve sedatif ilaçlara karşı daha fazla hassasiyet gösterirler. Bu artmış hassasiyet değişmiş farmakokinetik ve/ veya farmakodinamik sonucu gerçekleşir. Örneğin yaşlı hastalar etomidata karşı daha hassastır; ancak bu ilacın dağılım hacminin azalmasına bağlı plazma konsantrasyonunda oluşan artışa bağlıdır. Yaşla etomidata karşı beyin hassasiyeti değişmemiştir; eşit plazma konsantrasyonlarında yaşlı ve genç hastalarda benzer EEG değişimleri gözlenir. Benzer durum tiopental için de geçerlidir. Ancak propofol hassasiyeti hem farmakokinetik hem de farmakodinamik nedenlere bağlı olarak artmıştır; bu durum yaşlı hastalarda klirens azalması ve propofole beyin hassasiyetinin artmasından kaynaklanır. Hem etomidat hem de propofol gama-aminobütirik asit tip A reseptörü üzerinde etki göstermesine rağmen, yaşlı hastalarda propofole hassasiyet artarken etomidata karşı değişmemesi ilginçtir. Bu nedenle yaşlılarda indüksiyon ilaçlarının bolus dozlarının yavaş olarak enjekte edilmesi (>30 saniye içinde), böylece hipotansiyon gibi yan etkilerin engellenmesi önerilir.
Kardiovasküler İlaçlar:
Beta blokerler yaşlı hastalarda gerek iskemik kalp hastalığı, gerekse kronik kalp yetmezliği için giderek daha sık kullanılmaktadırlar. Dahası, perioperatif beta blokaj kardiyak olmayan cerrahiye verilen orta-, yüksek riskli hastalarda sıklıkla önerilmektedir. Yaşlılarda, genel olarak beta blokerlerin yarı ömrü uzamış, klirens azalmıştır. Ancak metoprolol bu konuda bir istisnadır, bahsedilen parametrelerde bir değişiklik meydana getirmez. Daha önce bahsedildiği gibi, yaşlı hastalar adrenerjik reseptörlerdeki “down-regulasyon” nedeniyle bazı beta blokerlere daha fazla duyarlılık gösterebilirler. Esmolol çok kısa bir yarı ömre sahip olduğundan bu değişimlerden klinik olarak etkilenmez. Dahası, bu ilaçlar çoğu zaman etkiye göre (kalp hızı) titre edildiğinden, doz hatası en aza indirilmiş olur.
Pek çok sınıf I antiaritmik ajan (örneğin lidokain) için, azalmış klirens ve uzamış yarı ömür nedeniyle daha düşük intravenöz doza ihtiyaç duyulur (ancak lokal anestezi için verilen lidokain dozunun azaltılmasına gerek yoktur). Benzer şekilde hepatik eliminasyona uğrayan bazı kalsiyum kanal blokerlerinin (diltiazem, nifedipin, verapamil) etki süreleri uzadığından, dozlarda azaltmaya gidilmesi önerilir.
Digoksin primer olarak böbrek yoluyla atılır, bu nedenle yaşlılarda yarı ömrü uzamıştır. Bu durum azalmış dağılım hacmi ile beraber geriatrik hastalarda doz azaltılmasını gerekli kılar. Diğer inotropik ve vazoaktif ilaçlar (ör: dopamin, dobutamin) pek çok sistemde eliminasyona (hepatik, renal, plazma ve diğer dokular) uğrayabilirler, ancak bu sistemlerin fonksiyonlarında meydana gelen azalma, ilaçların etkiye göre titre edilmeleri nedeniyle çoğu zaman sorun yaratmaz.
Opioidler:
Fentanil yağda çözünürlüğünün yüksek olması nedeniyle çabuk etki gösteren, bu nedenle de perioperatif dönemde sık tercih edilen bir ajandır. Fentanil yüksek oranda karaciğerden ekstrakte edilir, buna bağlı olarak da klirensi karaciğer kan akımına bağlıdır. Ancak farmakokinetik çalışmalar tam olarak yaşın fentanil plazma konsantrasyonlarını etkilediğini gösterememiştir. Farmakokinetik konusundaki bilinmezliklere rağmen, artan yaşla fentanil dozlama ihtiyacın azaldığı gösterilmiştir. Scott ve Stanski 20 ila 89 yaşı kıyaslandığında doz ihtiyacının neredeyse %50 azaldığını bulmuşlardır. Bu hastalarda farmakokinetik değişikliklerde pek farklılığa rastlanmaması, ana sorunun farmakodinamik özelliklerden kaynaklandığını düşündürmektedir. Benzer şekilde sufentanil ve alfentanil de yaşla beraber duyarlılıkta %50 artışla kendini göstermektedir. Bu nedenle bu ilaçları kullanırken geriatrik hastalarda klinisyenler dozları yaklaşık %50 azaltmalıdırlar. Son olarak fentanil ve benzodiazepinlere artmış hassasiyet, özellikle bu iki ilaç birlikte kullanıldığında oluşan sinerji ile spontan soluyan hastalarda ağır hipoventilasyona neden olabilir.
Remifentanil doku ve kan esterazları tarafından yıkılması nedeniyle dakikalar içinde etkisi sonlanan bir opioiddir. Bu esterazlar da yaşla azalır; ancak 20 ila 80 yaşı arasında remifentanil klirensi yaklaşık %30 azalmasına rağmen etkide klinik olarak çok önemli uzama gözlenmez. Karaciğer ve böbrek, remifentanil klirensini pek etkilemez. Yaşlı nüfusta dağılım hacminin yaklaşık %20 azalması nedeniyle, remifentanil verilmesini takiben daha yüksek tepe konsantrasyonları gözlenebilir. Bu nedenle yaşlı hastalarda ağır hipotansiyon ve bradikardiden kaçınmak için özellikle bolus injeksiyon yapılmamalıdır. Yaşlı hastalar ayrıca remifentanilin hipnotik etkilerine çok daha hassastır. EEG depresyonu oluşturmak için gerekli remifentanil plazma konsantrasyonu yaklaşık %50 azalmıştır.
Morfinin dağılım hacmi de, plazma klirensi de yaşlı hastalarda yaklaşık %50 azalmıştır. Dahası azalmış glomerüler filtrasyon nedeniyle aktif metabolitleri olan morfin-3 ve morfin-6 glükuronid eliminasyonu azalmıştır. Bahsedilen farmakokinetik değişimlere bağlı olarak yaşlılarda morfin duyarlılığı artmıştır. Klinisyenler özellikle ilk verdikleri morfin yükleme dozunu azaltmalıdırlar. Bunun dışında, yaşlılarda HKA (hasta kontrollü analjezi) yöntemi ile analjezi yapılıyorsa morfin için kullanılan bazal ve bolus dozları da azaltılmalıdır.
Nöromusküler blokerler:
Genel olarak yaşlılarda nöromusküler blokerlerin etki başlama süreleri uzamıştır. Bunun da temel nedeni yaşlanmaya bağlı olarak kardiyak debinin ve kas kan akımının azalmasıdır. Yaşlı hastalarda vücut suyu azaldığından ve pek çok kas gevşeticinin de iyonizasyon derecesi yüksek ve suda çözünürlüğü daha fazla olduğundan, kas gevşeticilerin verilen doza karşı gözlenen etkisi daha yüksektir. Hepatik veya renal atılım ile elimine olan kas gevşeticilerin (örn. vekuronyum, rokuronyum) yaşlılarda etki süreleri uzarken, diğer yollarla elimine olan ajanlarda (örn. atrakuryum, sis-atrakuryum) aynı uzama gözlenmez. Derlenme indeksleri (%75 bloktan %25 bloğa kadar geçen süre) hepatik ve renal atılım gerektiren kas gevşeticiler için yaşlılarda %200’e kadar uzamıştır. Örneğin vekuronyum için genç hastalarda derlenme süresi 15 dakika iken, bu süre yaşlılarda 50 dakikayı, rokuronyum için 13 iken 22 dakikayı, pankuronyum için ise 40 iken 60 dakikayı bulabilir. Son olarak kas gevşeticilerdeki bu değişikliklerden farmakodinamik değil, farmakokinetik farklılıklar sorumludur.
Pankuronyum protipik steroid-kökenli kas gevşeticidir ve eliminasyonu %70 oranında renal atılımla gerçekleşir. Yaşlılarda glomerüler filtrasyon ve renal kan akımının azalmasına bağlı olarak pankuronyumun etki süresi uzar. Vekuronyum yapı olarak pankuronyuma benzer ve minimal metabolik yıkılma sonucu safra ve idrar yoluyla atılır. Hepatik kan akımı ve kapasitesinde yaşa bağlı değişikliklerle, azalmış renal fonksiyon vekuronyum klirensini %30 ila 50 azaltır. Rokuronyum farmakolojisi de yaşlılarda, temel atılım yollarının safra ve idrar olması sebebiyle vekuronyuma benzer. Bu nedenle yaşlılarda rokuronyum etki süresi uzamıştır. Ancak vekuronyumdan farklı olarak rokuronyumda aktif metabolitler üretilmez. Özetle steroid-kökenli kas gevşeticiler, genç hastalara kıyasla yaşlılarda daha uzun etki süresine sahiptir. Bu bilgi, azalmış dağılım hacmi de göz önüne alınarak düşünüldüğünde yaşlılarda idame doz miktar ve sıklığının azaltılması gerektiğini gösterir.
Benzilizokinolinyum grubu olan ilaçlar (atrakuryum, sis-atrakuryum, mivakuryum) ise farklı eliminasyon yolları gösterirler. Mivakuryum plazma psödokolinesterazlarınca parçalanır. Atrakuryum ve sis-atrakuryum için ise ön planda olan Hofman eliminasyonu ve ester hidrolizi söz konusudur. Sis-atrakuryumun büyük kısmı bu yolla parçalanırken (yaklaşık %80’i), atrakuryum klirensinin bir kısmı hepatik metabolizmalara dayanır. Yaşlanma ile atrakuryum ve mivakuryumun etki süreleri uzarken, sis-atrakuryumun etki süresinde pek değişiklik gözlenmez.
Depolarizan kas geveşetici olan süksinilkolinin ise hızla psödokolinesterazlar tarafından parçalanması nedeniyle etki süresinde yaşla pek değişiklik gözlenmezken, etkinin başlama süresi yaşlılıkla beraber kalp debisinin azalması sonucu uzayabilir.


