 Çeşitli nedenlere bağlı solunum ve kalp durması sonrasında uygulanan kardiyopulmoner resüsitasyon (KPR) ile her yıl çok sayıda insan yeniden hayata dönmekte. Peki yaşamları eski akışına dönüyor mu, yaşam kalitesi ne oluyor??
Çeşitli nedenlere bağlı solunum ve kalp durması sonrasında uygulanan kardiyopulmoner resüsitasyon (KPR) ile her yıl çok sayıda insan yeniden hayata dönmekte. Peki yaşamları eski akışına dönüyor mu, yaşam kalitesi ne oluyor??
European Resuscitation Council KPR’de başarıyı ve sağkalımı arttırmak için yapılan çalışmalar ışığında 2005 yılında uygulama rehberini yeniledi . KPR sırasında kaybedilen zamanı azaltmak ve etkinliği arttırmak için KPR algoritması pratikleştirildi. Hızlı tanı + erken başlanan KPR ve erken defibrilasyonun önemi bu rehberde öne çıkan bölümler. 30 kalp masajı : 2 solunum oranının daha etkin dolaşımı sağladığı bildirildiği için algoritma buna göre değiştirildi.
Son yıllarda serebral hipoksi sırasında ortaya çıkan patolojik olayların post-arrest döneme de uzandığı ve hücre hasarını, nöron ölümünü arttırdığı belirlendi. Bu nedenle arrest sırasında başlayan fizyolojik destek ve bakım arrest sonrası dönemde de aynı yoğunlukta devam ettirilmek zorunda. Çalışmalar bu bakımın parçası olarak uygulanan hafif terapötik hipoterminin (TH) erişkin ve perinatal asfiksi vakalarında yararlı olduğunu gösterdi. Ancak ağır travmatik beyin hasarında TH’nin yararına ilişkin kanıt henüz yok.
BJA’nın mayıs 2008 sayısında arrest sonrası nörolojik defisi azaltmak amaçlı çalışmalar üzerine bir derleme yayınlandı. Yazıda özellikle post-arrest TH üzerinde durulmakta.
Terapötik Hipotermi
1950’li yıllarda kardiyak arrest geçirmiş ve 24-72 saat boyunca 32-34°C’lık hipotermi uygulanmış 4 vakadan üçünün iyi nörolojik sonuçları olduğu bildirildi. Bunu uzun arrest ve resüsitasyon sonrası TH uygulanan ve sağkalım bildirilen bir dizi vakalar ve hayvan çalışmaları izledi. TH’nin nöronal fonksiyonu koruyucu etkisi düşük debi veya orta dereceli (28-33°C) ya da derin hipotermik (16-28°C) sirkülatuar arrest ile yapılan çeşitli nöroşirürji ve kalp ameliyatlarında gösterilmiş durumda. Ancak insanlarda arrest sonrası hipotermi uygulaması ile ilgili ilk çalışmalarda ısınma (re-warming) döneminde infeksiyon, aritmi, koagülopati gibi yan etkilerin çok sık olduğu izlenmekte.
1997’de TH uygulaması ile ilgili ilk prospektif seride hastane dışında kardiyak arrest olan 22 hastada nörolojik sonucun daha iyi olduğu bildirildi. Bunu izleyen randomize konrollü ancak körleştirilmemiş iki seride spontan dolaşımı dönen ama komada kalan hastalarda TH uygulamasının olumlu nörolojik sonuç insidansını normotermiye oranla arttırdığı gösterildi (Bir seride TH grubunda olumlu nörolojik sonuç %55, normotermi grubunda ise %39 bulunurken, diğer seride bu oranlar sırasıyla %49 ve %26 idi). Her iki seride de komplikasyon açısından normotermi ve TH arasında istatistiksel fark bulunmadı.
Nöronal Hasarın Patofizyolojisi
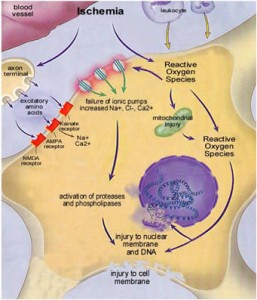 Nöronal fonksiyonun, hücresel detoksifikasyonun ve membran bütünlüğünün devamlılığı için beyin kesintisiz oksidatif metabolizmaya bağımlı. Serebral perfüzyon kardiyak debinin %20’sini almakta ve 750-1000 ml/dak. Oksijen tüketimi ise her 100 gr beyin dokusu için 3.5 ml/dak. Her ne kadar bir miktar anaerobik metabolizma mümkün olsa da, beyinin oksijen deposu olmadığından dolaşımın kesintisiz sürmesi şart. Oksijen sunumu 2 ml/100 gr/dak’nın altına indiğinde bilinç kaybı oluyor ve hipoksik iskeminin derecesine göre nöron hasarı gelişiyor.
Nöronal fonksiyonun, hücresel detoksifikasyonun ve membran bütünlüğünün devamlılığı için beyin kesintisiz oksidatif metabolizmaya bağımlı. Serebral perfüzyon kardiyak debinin %20’sini almakta ve 750-1000 ml/dak. Oksijen tüketimi ise her 100 gr beyin dokusu için 3.5 ml/dak. Her ne kadar bir miktar anaerobik metabolizma mümkün olsa da, beyinin oksijen deposu olmadığından dolaşımın kesintisiz sürmesi şart. Oksijen sunumu 2 ml/100 gr/dak’nın altına indiğinde bilinç kaybı oluyor ve hipoksik iskeminin derecesine göre nöron hasarı gelişiyor.
Arrest sırasında başlayan nöronal hasar bunu izleyen 72 saate dek oluşmaya devam ediyor ve erken nekroz ve geç apoptotik nöron ölümü ile sonuçlanıyor. Serebral hipoperfüzyon sonucu ATP üretimindeki ciddi azalmaya bağlı ağır iskemi membran bütünlüğünün bozulmasına ve nekroza yol açıyor. Membranın yıkılması ile gelişen Na+/K+ pompası yetersizliği trans-membran iyon gradiyenti ve sellüler depolarizasyonu ortadan kaldırıyor. Ayrıca fosfolipazların aktivasyonu ile oluşan lipoliz ile araşidonik asit, glutamat ve diğer toksik eksitatuar nörotransmitterler serbestleniyor ve sonuçta intranöronal Ca2+ konsantrasyonunda ani artış oluyor.
Reperfüzyon hasarı bir çok yandaş mekanizmanın rol aldığı apoptoz ve oto-fagositoz ile geç nöronal ölüme neden oluyor. Bunlardan birisi kan-beyin bariyerinin yıkılması; gelişimi reperfüze dokudaki lökosit kökenli mediatörlerin, nitrik oksit (NO) ve peroksinitrit gibi reaktif oksijenlerin (reactive oxygen species, ROS) ve proteazların katıldığı inflamatuar cevap ile açıklanıyor. İnflamatuar sitokinler (TNF, IL-1, IL-6, IL-8, IL-10) lökositleri aktive ederek, damar geçirgenliğini arttıran ve kan-beyin bariyerini hasarlayan toksik matriks metalloproteinazları aktive ediyor. İnterstisyel sıvı kaçağı difüzyon mesafesini arttırıyor, mikrovasküler perfüzyonu bozuyor ve oksijen değişimi yetersiz hale gelirken, toksik atık ürünler de kardiyak arrest sırasında birikiyor. Gelişen yaygın mikst vazojenik ve sitotoksik beyin ödemi serebral perfüzyon basıncını daha da düşürüyor ve reperfüzyon hasarına katkıda bulunuyor. NO sentetazın iskemik up-regülasyonu ile ROS artıyor; ROS intrasellüler asidoza neden oluyor, nöronal endonükleaz ve sistein proteazı aktifliyor. Hücre içi asidozun primer kaynağı anaerobik glikoliz ile aşırı miktarda üretilen ve etkin şekilde temizlenmeyen laktat. Mitokondriyal yıkım sonucu gelişen ATP açığı nedeniyle hücresel iyon dengesi ve Na+/K+ pompa fonksiyonu bozuluyor; intrasellüler su ve Na+ girişi membrandaki elektrokimyasal gradyentin kaybına ve nöronal membran depolarizasyonuna neden oluyor. Bu durum bol miktarda glutamat ve N-methyl-D-aspartat gibi diğer toksit eksitatuar aminoasitlerin salınımını tetikliyor ve bunlara bağlı olarak iyon kanallarının açılması ile intrasellüler alana Ca2+ girişi daha da artıyor. Ca2+ fazlalığı intrasellüler proteazları aktifleyerek hücre iskeletinin hasarını daha da arttırıyor ve ROS sentezini indüklüyor.
Hipoterminin Etkileri
İndüklenmiş hafif terapötik hipertermi resüsitasyon sonrası dönemde bir takım yararlı etkiler sunmaktadır. Her 1°C sıcaklık düşüşü için serebral metabolik hızın (CMRO2) %6 kadar azaldığı kabul edilmektedir. Nedeni hücresel metabolik işlemlerin ve ATP tüketiminin azalmasıdır. Böylece hücre içi asidoz azalmakta, glukoz metabolizması düzelmekte, eksitatuar aminoasitlerin salınımı baskılanmaktadır. Hafif hipotermi iskemi-reperfüzyona bağlı iyon dengesizliğini de iyileştirmekte ve membran stabilizan etkisi sayesinde hücre içi su ve iyon girişini engelleyerek beyin ödemini azaltmaktadır. Glutamat konsantrasyonu değişmemekte, kaspaz salınımı inhibe olmakta, serbest radikal üretimi düşmekte ve apoptozun şiddeti azalmaktadır. Ayrıca Ca’a bağlı proteaz aktivitesi ve sitokin cevabı azalmakta, sonuçta da geç hasara neden olan inflamatuar mekanizmalar baskılanmaktadır.
Klinik Özellikler
TH indüksiyon ve idamesinde invazif endovasküler (örnek bağlantıda) veya ekstrakorporeal sistemlerden veya non-invazif yüzeyel soğutuculardan yararalanılabilir. Her aletin avantaj ve dezavantajları bulunmaktadır ve hiçbirinin sonuç açısından üstünlüğü bildirilmemiştir. Modern aletlerde otomatik feedback mekanizması sayesinde merkez sıcaklık sabit sürdürülebilir. Basit bir hızlı iv soğuk sıvı infüzyonu verilerek hipotermi indüklenebilir.
Diğer Tedavi Yaklaşımları
Arrest sonrası hasarın patofizyolojisinin daha iyi anlaşılmaya başlaması ile beraber spesifik tedavi yaklaşımları üzerinde çalışılmaya başlanmıştır. Hücre içine Ca2+ girişinin modülasyonu ile ilgili çalışmalarda lidoflazin ve nimodipin sağkalım üzerine olumlu etki sağlamamışlardır. Mg-sulfat, Ca2+ blokeri olarak önemli rol oynasa da sonucu etkilememektedir. Lipid peroksidasyonu veya serbest radikal oluşumunu baskılama girişimleri de sonuç vermemiştir. Eksitatör aminoasitlerin etkisinin reseptör düzeyinde bloke edilmesi de sağkalımı etkilememiştir.
Mitokondrinin nöron ölümü ile sonuçlanan süreçte öncü rol oynadığı bilinmektedir. Mitokondriyal hasar erken olarak ve normal hücre fonksiyonuna dönüşün engellenmesi ile gelişmektedir. Yeni çalışmalar mitokondri fonksiyonunun korunmasını hedef almaktadır. TH ile co-enzim Q 10 (esansiyel bir mitokondriyal co-faktör) kombinasyonunun sağkalımı arttırabileceği düşünülmektedir.
Sonuç
Hafif TH’nin hastane dışı resüsitasyon (VF/VT sonrası kardiyak arrest) sonrası hastalarda sağkalımı olumlu etkilediğine dair kanıtlar vardır. ‘‘The International Liaison Committee on Resuscitation’’ yoğun bakıma alınma kriterlerine uyan hastalarda TH’nin endike olduğunu, hastane içi arrest vakaları ile VF/VT dışı ritm izlenmiş vakalarda da düşünülmesi gerektiğini bildirmiştir. Ama bu ikinci gruptaki hastalarla ilgili veri henüz yetersizdir. Soğutma için seçilecek metot ve optimal süre de netleşmemiştir. Daha fazla veri toplanana dek TH belki şimdilik yarar görecek vakalara, tanık olunmuş ve kısa sürede dönmüş arrestlere uygulanmalıdır. Serebral oksijen sunumu korunmalı ve komplikasyonlar en aza indirilerek TH’den elde edilecek yararlar netleştirilmelidir.