Yazar: mukadder
Aspirasyon ve Krikoid Bası
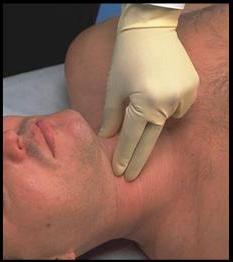 Uzun yıllardır aspirasyon riski yüksek hastalarda, hızlı sıralı indüksiyonun parçası olarak gebelerde uygulanan krikoid bası, bilinen adı ile Sellick Manevrası işe yaramıyor mu, yanlış mı uygulanıyor?
Uzun yıllardır aspirasyon riski yüksek hastalarda, hızlı sıralı indüksiyonun parçası olarak gebelerde uygulanan krikoid bası, bilinen adı ile Sellick Manevrası işe yaramıyor mu, yanlış mı uygulanıyor?
Son yıllarda aspirasyonun engellenmesi için gerekli manevralardan biri olarak tanımlanan krikoid basısı tekrar gündeme geldi ve yeni derlemelerle tartışmaya açıldı. Yakın zamanda Domino ve ark. 1990’dan günümüze, Amerika Birleşik Devletlerinde sonuçlanmış veya uzlaşmaya varılmış 129 aspirasyon olgusunun mahkeme kayıtlarını incelediklerinde aşağıdaki sonuçlara ulaşmışlar:
1. Mide içeriklerini aspire eden hastaların açtıkları davalardaki ölüm sıklığı, diğer tüm malpraktis davalarına kıyasla 2 kat daha fazla
2. Dahası aspirasyon vakalarının yarısında krikoid bası ve hızlı sıralı indüksiyon kullanılmış. Bu da krikoid basının etkinliğinin sorgulanmasına neden olmakta…
3. Bu çalışmada gözlenen aspirasyon yaşanan vakaların diğer malpraktis davalarındakine kıyasla daha yaşlı, daha hasta ve operasyonlarının daha acil olduğu gözlenmekte.
4. Bunun dışında abdominal cerrahi ve genel anestezi aspirasyon riskini arttıran diğer faktörler. Vakaların çoğu genel anestezi alırken (%88), bir miktar hastada (%12) aspirasyon propofol veya başka bir sedasyon ajanı altında sinir bloğu veya monitorize anestezi bakımı uygulanırken gerçekleşmiş.
5. Aspirasyon zamanı açısından en tehlike zaman indüksiyon (%60), ancak bir takım olgularda intraoperatif (%19), veya postoperatif (%12) zamanda da gerçekleşmiş.
6. Klinisyenler- tipik olarak anestezi asistanları veya hemşireler- aspire eden 36 hastada krikoid bası manevrasını uygulamışlar ancak uygulamalar ancak 10 hastada doğru şekilde gerçekleştirilmiş. Krikoid basının kullanılmadığı aspirasyon olgularında malpraktis davasındaki tazminatlar, uygulanan vakalara kıyasla çok daha yüksekmiş (513,125 dolar vs 211,500 dolar).
Şekil 1: Aspirasyon davaları ile diğer davaların kıyaslanması
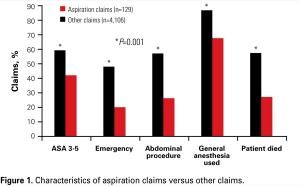
Peki o zaman sorun ne? Krikoid basının etkisiz olması mı, yoksa doğru uygulanamaması mı? ASA toplantısında sunulan bir abstrakta Chicago’lu araştırıcılar 1974’ten beri yapılan krikoid bası çalışmalarını (4 çalışma) bir meta-analizde incelemişler ve bu meta-analizde krikoid basının 87 hastadan 86’sında midenin hava ile dolmasını engellediği gösterilmiş. Araştırıcılar da, bu sonuçlarla krikoid bası elle ventilasyonda gastrik dolmayı bu kadar etkin şekilde engellerken, aspirasyon içeriğinin farinkse ulaşmasını engelleyememesinin inandırıcı olmadığını belirtmişler ve sorunun krikoid basının doğru uygulanmamasından kaynaklandığını dillendirmişler. Bunun nedeni aslında çok basit bir manevra olan krikoid basının iyi öğretilememesinden kaynaklanabilir. Manevranın etkinliği Florida’lı araştırıcılar (Anesth Analg 2009;109:1546-1552) tarafından 2009 yılında 24 uyanık gönüllüde MR görüntülemesi ile de, vertebra korpusuna göreceli olarak krikoid kıkırdak pozisyonu ne olursa olsun, özafagusun uygun yapılan krikoid bası ile sıkıştırabileceğini göstermişler.
Krikoid bası kuvveti ne olmalıdır?
Erişkinlerde havayoluna zarar vermeksizin etkin krikoid bası için gerekli basınç 30 newtondur (Bu yaklaşık 3 kg lık bir kuvvete eşdeğerdir). Çocuklarda, güvenli eşik değerinin daha düşük olduğuna inanılmaktadır çünkü krikoid kartilaj arkasında kalan alan erişkinlerden daha küçüktür.
Çocuklarda uygulanan basınç ile havayollarında çarpılma ihtimali olabileceği için pediatrik anestezistlerin bazıları artık bu manevrayı uygulamayı istememektedirler. Gerçektende yaşla birlikte uygulanacak basıncın değişmesi gerekebilir.
Şekil 2 : Yaşla birlikte %50 havayolunda kapanma için gerekli basınç değeri
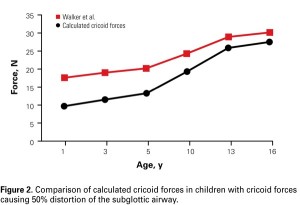
Sonuç olarak doğru uygulama ile işe yarıyor görüşüne karşı aspirasyonu önleyemiyor görüşünün çatışmasını bir süre daha izleyip günlük pratiğimizi ona göre yönlendireceğiz.
Yenidoğanda Analjezi-1
Bu ayın BJA: CEACCPM dergisinde yenidoğan analjezisi ile ilişkili çok güzel bir derleme yayınlandı. Uluslararası Ağrı Araştırmaları Teşkilatı (IASP) tarafından yapılan tanımlamaya göre ağrı; “Vücudun herhangi bir yerinden kaynaklanan, gerçek ya da olası bir doku hasari ile birlikte bulunan, insanın geçmisteki deneyimleriyle ilgili, duysal, afektif, hoş olmayan bir duyudur.” Yakın döneme kadar sinir sistemi gelişimi daha olgunlaşmamış olan yenidoğanın daha büyük çocuklar ve erişkinler gibi ağrıyı algılamadığı düşünülmekteydi. Bu görüşün bir sonucu olarak pek çok işlem çok az analjezi veya bazen hiç analjezi sağlanmaksızın gerçekleştirilmekteydi. Bunun dışında yenidoğanların kullanılan opioid komplikasyonlarına (özellikle de solunum depresyonuna) daha yatkın oldukları düşüncesiyle opioid kullanımından kaçınılmaktaydı.
1. Yeni doğanda ağrının algılanması için tüm fiziksel gereksinimler 25. Gestasyon haftasında tamamlanmaktadır. Ağrı yolakları incelendiğinde fetustaki talamokortikal bağlantıların gebeliğin 12-16 hafta arasında başladığını, bu ilişkilerin 23-25. Haftada olgunlaştığını görmekteyiz.
2. Ağrıyı algılayan sistemin eksitatör tarafı erişkinden farklı olsa da doğumdan itibaren fonksiyoneldir. Neonatal afferent yollar yüksek eşikli A delta ve erişkine kıyasla uyarılmaya karşı daha az ateşleme frekansıyla cevap veren düşük eşikli A beta mekanoreseptörlerden oluşmaktadır. Erişkinlerde A beta afferentleri dorsal boynuzun III ve IV. Laminasına uzanırken, yenidoğanda bunlar C fiberleriyle beraber lamina I ve II’ye uzanmaktadırlar. Bunun dışında dorsal boynuz ve kortikal somatosensoriyel hücrelerin algılayıcı kısımları daha geniştir ve bu nedenle periferik duysal uyarılarla harekete geçme ihtimalleri daha fazladır.
3. Ağrıyı algılayan sistemin inhibitör koluna baktığımızda ise durumun tersini görürüz. Preterm infantlarda term infantlara kıyasla dorsal kutanöz fleksör refleks ağrıya neredeyse 2 kat daha hassastır. Term infantlarında daha büyük çocuklara kıyasla ağrıya daha hassas olduğunu gözlemleriz. Bu supraspinal merkezlerle dorsal kök hücrelerini birleştiren inen inhibitör nöronların yokluğuyla açıklanabilir. Her ne kadar GABAerjik sinapsları kullanan ve spinal kord düzeyinde GABA/glisin sinapsları ile nöronal uyarılabilirliği azaltan fonksiyonel bir inhibisyon sistemi olsa da bu sistem de daha büyük çocuklardaki kadar etkin değildir.
4. Neonatal dönemde yaşanan ağrı deneyiminin daha sonraki yaşamda gözlenen duysal ve motor cevapları değiştirdiğine dair kanıtlar bulunmaktadır. Örneğin yapılan bir çalışmaya göre sünnet uygulanan çocukların 4-6 aylıkken aşılamaya karşı davranışları değişmektedir. Sünnet yapılamamış çocuklarda aşılama yapıldığında düşük ağrı skorları gözlenirken, sünnet için plasebo uygulanmış çocuklarda aşılama sırasında en yüksek ağrı skorları izlenmektedir. İkinci deneyimin doğası (yani hipo veya hiperaljezi cevabı) daha çok ilk ağrı deneyiminin yaşandığı yaşa bağlıdır. Ağrılı uyarıya maruz kalmış preterm infantlarda sonraki zamanlarda hipoaljezi gözlenirken, postterm infantlarda hiperaljezi gözlenmektedir.
Gelişimsel farmakoloji:
Analjezik ilaçların dozu gestasyonel yaş ve postnatal gelişim ile farklılık göstermektedir. Farmakokinetik değişkenler bir çok faktörden etkilenir. Bunlar:
1. Yenidoğanların total vücut su içeriği yüksektir ve bunun en önemli yüzdesi ekstrasellüler aralıkta bulunmaktadır. Vücut yağ ve kas içeriği ise daha düşüktür. İyonize ilaçlar bu nedenle daha büyük dağılım hacmine sahipken, yağ ve kasa tekrar dağılabilen ilaçların etki süreleri uzundur.
2. Doğumda glomerüler filtrasyon hızı düşük ve renal tübüler fonksiyonlar gelişmemiştir. Bu da ilaçların renal yolla atılımını azaltır ve ilaçların yarılanma ömrünü arttırır.
3. Plazma protein konsantrasyonundaki değişimler ilaçların bağlanmasını ve dolaşım hacmini etkiler. Serbest ilaç miktarı arttıkça, ilaç etkisi için gerekli doz azalır.
4. Karaciğere ilaç alımı ve metabolik enzim aktivitesi erişikine kıyasla daha az etkindir ve bu nedenle ilaç etki süresi uzar.
5. Kan beyin bariyeri nispeten olgunlaşmamıştır ve bu nedenle morfin gibi kısmen iyonize ilaçların beyne geçişi artar.
Analjezi stratejileri:
Analjezi uygulamalarında ilk dikkat edilecek nokta yenidoğanın ağrı çektiği zamanların farkına varmamızdır. Her ne kadar postop ağrı fark edilip sıklıkla tedavi edilse de, topuktan kan alma işlemi için iğne batırma önemsenmeyebilir. Oysa böyle bir işlem öncesi 15 dakika cilt ile temas veya emzikle/emziksiz %24 ‘e varan konsantrasyonlarda sukroz çözeltisi, iğne batırma acısının uzun dönemli etkilerini en aza indirgeyecektir. Oral sukroz verilmesi dil üzerindeki tatlı tat reseptörlerince uyarılan endorfini harekete geçirir.
Bunun dışında venoponksiyon için lokal anestetik(LA) içeren kremler (EMLA gibi) kullanılabilir. Bu ester LA’lerin yenidoğan içi teorik avantajı esterazların sisteminin tüm işlevini görmesidir. Ancak bu uygulamalarda uygulanan doza ve karışımın uygulandığı yerin üstünün kapalı olmasına dikkat etmek gerekir. EMLA kremi için methemoglobinemi komplikasyon korkusunun sadece venoponksiyon için kullanımda abartılı olduğu düşünülmektedir.
Sistemik analjezikler analjezi tedavisinin en etkin kısmını oluşturur ve gerektiğinde rejyonel anestezi uygulamalarıyla birlikte kullanılır. En sık kullanılan ilaçlar asetaminofen ve kodein fosfattır. Yenidoğan ağrı tedavisinde non-steroid anti-inflamatuar ajanlar tartışmalıdır. Yenidoğan uzmanları indometazin ve ibuprofeni duktus arteriosusun kapanmasını çabuklaştırmak için kullanırlar. Prostaglandinler santral sinir sistemi, kardiyovasküler ve renal sistemin gelişimi için önemlidir ve in utero yada neonatal dönemde NSAİD maruziyeti bu sistemleri bozabilir. Prostaglandin inhibisyonun fizyolojik etkileri uyku düzensizliği, serebral kan akımında değişme, azalmış renal kan akımı, bozulan termoregulasyon ve artmış pulmoner hipertansiyon riski olarak sıralanabilir.
Asetaminofen:
Asetaminofenin hem analjezik hem de antipiretik etkileri vardır ancak anti-inflamatuar etkisi çok zayıftır. Astaminofen inen seratoninerjik yolaklar üzerinden santral analjezik etki gösterir. Temel etki mekanizmasının prostaglandin sentez inhibisyonu veya kannabinoid reseptörlerine etkin bir aktif bileşeni olduğu düşünülmektedir. Antipiretik ve analjezik etkinliği gözlemek için plazma konsantrasyonunun 10-20 mg/mL olması gerekir. Asetaminofen temel metabolizması yenidoğanda erişkindeki gibi glukuronidizasyon değil, sülfat konjugasyonu üzerindendir. Glukuronidazyonun sülfat konjugasyonuna oranı erişkinde 2:1 ‘dir ve bu orana ancak 12 yaşında erişilir. Asetaminofenin küçük bir miktarı (%3-10) sitokrom p-450 enzimleriyle potansiyel hepatotoksik bir metabolit olan N-asetil-r-benzokinin imine dönüştürülür. Bu metabolit hepatik glutatyon tarafından etkisizleştirilir ve kronik maruziyet yada ileri malnütrisyon nedeniyle glutatyon depoları azaldığında karaciğer hasar ihtimali artar. Metabolizma için gerekli bu izoenzimin aktivitesi yenidoğanda azalmıştır ve bu da hasara karşı bir miktar koruma sağlar.
Asetaminofen oral, rektal veya i.v. yolla verilebilir. Kullanılabildiği sürece enteral yol kullanılabilmelidir, burada da rektal biyoyararlanım büyük çocuklara kıyasla daha fazladır (neredeyse %100’e yaklaşır). Parenteral asetaminofen cerrahiden sonraki ilk 24 saatlik dönemde daha sık kullanılır, daha sonrasında oral dozlara geçilir. Oral ve parenteral dozlar birbirine eş değildir ve buna dikkat edilmesi gerekir. Asetaminofen tek başına veya kodein fosfatla beraber kullanılabilir.
Kodein fosfat:
Kodeinin analjezik etkinliğini sağlayan mekanizma morfine dönüşümüdür ve bu da karaciğerde bulunan sitokrom p-450 enzimi olan CYP2D6 enzimi tarafından gerçekleştirlir. Enzimik genetik polimorfizmi hastadan hastaya ciddi değişkenlik gösterir. Enzim aktivitesi doğuşta son derece düşüktür ve yaşla birlikte artar. Bu da kodein kullanımının yenidoğan ve süt çocuklarında etkin olmayacağını düşündürmektedir. Ancak kodein ve asetaminofenin beraber kullanıldıklarında infantta postop analjeziyi sağladıkları gösterilmiştir. Kodein oral, rektal, veya nadiren anestezi altında i.m. olarak verilebilir. Oral ve rektal yolla verildiğinde emilim hızlıdır ve tepe plazma konsantrasyonlarına 1 saat içinde ulaşılır. Histmin kaynaklı olduğu düşünülen ciddi hipotansiyon nedeniyle asla intravenöz verilmez. Kodeinin yarı zamanın düşük doğum tartılı yenidoğanlarda arttığı gösterilmiştir ve bu nedenle dozlar arasında daha uzun aralıklar bırakılmalıdır.Gerek kodein, gerek asetaminofen ile ilişkili doz tabloları yukarıdaki bağlantıda verilmektedir.
Post-Operatif Rezidüel Kürarizasyon
Postoperatif Rezidüel Kürarizasyon (PORC) tanım olarak post-operatif hastada halen bloke kalmış nikotinik reseptörlerin varlığıdır. Bu durumun herhangi bir semptoma yol açmadığı durumlarda dahi reseptörlerin %60-70’inin halen kürarize kalmış olabileceğini aklımızdan çıkarmamalıyız. Etkisi ortadan tam kalkmayan kas gevşeticiler:
1. TOF>0.7 olduğunda bile solunum kasları fonksiyonlarını tam kazanmış olsalar da üst havayolu açıklığı tam sağlanamayabilir; aspirasyon gerçekleşebilir.
2. Hipoksiyi algılayan periferik kemoreseptörleri etkileyerek, hipoksik solunum uyarısını bozabilirler.
Bu nedenle PORC, hastaların geç derlenmesinden hipoksiye, metabolik bozulmalardan nadiren ölüme kadar problemlere yol açabilir. Bu yüzden yakın takip ve önleyici tedbirlerin alınması elzemdir.
PORC’dan sakınmak için hastalara nöromusküler stimülasyon testleri yaparak kantitatif, klinik bazı testler uygulayarak da kalitatif değerlendirmeler yapılmalıdır. Kantitatif ölçümlerden en sık olanı TOF (Dörtlü uyarı) skorunun ölçülmesidir. Günümüzde hastaların kas gevşetici etkisinden “servise gedebilecek kadar kurtulmuş” kabul edilebileceği minimum TOF değeri %90’dır. Klinik gözleme dayanan testlerden ise güvenilir ve güvenilir olmayanlar aşağıdaki tabloda incelenmektedir.
Güvenilir olmayan Testler;
Sürekli göz açıklığı, dilin dışarı çıkarılması
Kol ile karşı omuza dokunulması
Normal(-e yakın) Vital Kapasite
İnspiryum basıncı < -25 mbar
Güvenilir Testler;
5 sn. süreyle baş ve/veya bacak kaldırabilmek
5 sn. süreyle el sıkabilmek
Dil basacağı testini başarabilmek (hasta 2 çenesinin arasına konulan bir dil basacağını ısırır ve geri çekip, bunu ağzından almanıza izin vermez)
İnspiryum basıncı > -50 mbar
PORC için ABD’deki genel insidansın %30-50 arasında olduğu düşünülecek olursa, uyanma odalarına gelen her 2-3 hastadan birinin ciddi risk altında olduğunu net olarak söylenebilir. PORC riskini arttıran nedenler arasında yetersiz nöromusküler monitörizasyon ve yetersiz dekürarizasyon sıralanabilir. Ayrıca, ekstübasyon sonrası volatil gazların artık etkileri ve/veya post-op analjezide kullanılan opioidlerin solunumu deprese edici etkileri nedeniyle ortaya çıkan hipoventilasyon ve buna bağlı respiratuar asidoz da önemli sebeplerdendir. Diğer nedenler arasında ise derin nöromusküler blok, hipotermi, elektrolit bozuklukları (Hipokalemi, Hipokalsemi, Hipermagnezemi), ilaç etkileşimleri (aminoglikozit grubu antibiyotikler) ve bazı yandaş hastalıkların varlığı sayılabilir.
Uygun monitörizasyon ve klinik değerlendirmelerin sonucunda PORC ihtimalini öngördüğümüz hastalara mutlaka dekürarizasyon yapılmalıdır. Geleneksel dekürarizasyon için kolinesteraz inhibitörü ajanlar kullanılmaktadır. Bu ajanlar nöromusküler kavşaktaki Ach yıkımını sağlayan asetilkolinesteraz enzimini inhibe ederler. Böylece kavşakta bulunan Ach miktarının artmasını ve dolayısıyla nöromusküler bloker ajanların kompetitif antagonist etkisine karşın agonist cevabın restorasyonunu sağlarlar.
Bu ajanlar arasında neostigmin en potent ve selektif olanıdır. Bu noktada selektivite (seçicilik); nikotinik etkinliğin muskarinik etkinliğe üstünlüğü ve asetilkolinesteraz enzim inhibisyonunun psödokolinesteraz enzim inhibisyonundan fazla oluşu olarak tanımlanabilir.
Kolinesteraz inhibitörü ajanların birçok istenmeyen etkilerinin varlığı da akıldan çıkarılmamalıdır. Özellikle bu ajanların tam nikotinik selektivitelerinin olmayışından dolayı muskarinik sistemi de uyarmaları nedeniyle ciddi sayılabilecek birçok istenmeyen etki ile karşılaşılabilir. Bunlar arasında bradikardi, QT uzaması, bronkokonstriksiyon, hipersalivasyon, motilite artışı vb. sayılabilir. Bu etkilerden sakınmak için dekürarizasyon işlemi, bir antikolinerjik ajanın (atropin, glikopirolat vb.) birlikte kullanımı ile yapılır.
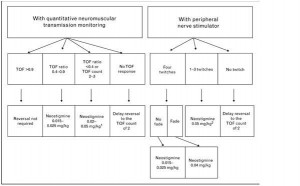
Dekürarizasyon işlemi için neostigmin dozunu nöromusküler blokajın derinliğine göre belirlemek uygun olacaktır. Blokajın derinliğini kantitatif ve kalitatif olarak değerlendirmek mümkündür. Kantitatif olarak TOF monitörizasyonunu, kalitatif olarak da periferik sinir uyarımını kullanmak uygun seçeneklerdir. Bu bilgiler ışığı altında hazırlanan dekürarizasyon algoritmlerinden birisi aşağıdaki şema ile gösterilmiştir.
Dekürarizasyon ile ilgili dikkat edilmesi gereken bir diğer nokta da neostigmin dozudur. Dozun düşük kalması durumunda hastanın önce dekürarize olması, ancak ardından neostigminin etki süresi dolduktan sonra ortamda hala kas gevşetici bir ajanın (orta-uzun etkili) varlığı, hastanın re-kürarize olmasına ve buna bağlı ciddi problemlere neden olabilir. Diğer yandan, neostigmin dozunun yüksek (>5mg) olması da ortamda Ach’in aşırı derecede artmasına ve reseptörlerin kontrolsüz depolarizasyonuna bağlı depolarizan blok oluşmasına yol açabilir. Bu sebeplerden ötürü, hastalar dekürarize edildiğinde dahi tedbirli davranmaya ve uygun gözlemleri yapmaya devam edilmelidir.
Günümüzde Kolinesteraz inhibitörleri ile yapılan geleneksel Dekürarizasyon işlemine güncel bir alternatif sunulmaktadır. Uzun yıllardır bilinen siklodekstrin moleküllerinin dekürarizasyon için de kullanılabileceği uzun çalışmaların ardından ortaya konmuştur. Siklodekstrinler dışları hidrofilik, içleri lipofilik olan ajanlardır. Bunlar, maddeleri “moleküler enkapsülasyon” ile içlerine hapsederek suda eriyebilir hale getirip hızlıca idrar yoluyla atılabilmelerini sağlarlar. Aminosteroid yapılı nöromusküler blokörler olan roküronyum ve veküronyum’a selektif olarak geliştirilen Sugammadex isimli ajan, 8 adet glukoz monomerinin silindirik bir şekilde dizilmesiyle meydana gelmiş bir siklodekstrin’dir. Plazmada bir sugammadex molekülü yine bir roküronyum veya veküronyum molekülünü mekanik olarak bağlar ve bu ajanların plazma konsantrasyonlarında düşüşe sebep olur. Oluşan gradient ile tüm ekstravasküler bölgelerden kana doğru roküronyum / veküronyum geçişi olur. Bu yolla hızlı bir atılım ve dekürarizasyon sağlanır. Bu mekanizma ile oluşan dekürarizasyonda rekürarizasyon ve muskarinik yan etkiler beklenmez. Sugammadex birkaç yıldır Avrupa’da kullanılmakta olup, ABD için FDA onayı beklemektedir. Ülkemizde ise yakın dönemde piyasaya sürüleceği söylenmektedir.
Sugammadex’in klinik etkinliğini değerlendiren araştırmalardan örnekler vermek gerekirse;
Gijsenbergh ve arkadaşlarının çalışmasında 0,6 mg/kg roküronyum ile entübe edilen hastalarda 1,0 – 8,0 mg/kg sugammadex ile plasebo karşılaştırılmış, plasebo ile 52 dakikada derlenebilen (TOF > 0,9) hastalar, 8,0 mg/kg sugammadex ile ortalama 1 dakikada derlenmişlerdir. Shields ve arkadaşlarının çalışmasında ise 0,6 mg/kg rokuronyum yapıldıktan sonra hastalarda spontan T2 (2. twitch) beklenmiş, sonrasında 0,5 – 6,0 mg/kg sugammadex uygulanmıştır. TOF > 0,9 olması, 6,0 mg/kg dozu için 3 dakikadan kısa, 0,5 mg/kg dozu için ise ~ 7 dakika sürmüştür. Khuenl-Brady ve arkadaşları ise, derin roküronyum bloğunda (1,2 mg/kg) sugammadex’in 8-16 mg/kg dozlarında uygulanmasıyla ortalama 2,5 dakikada derlenme gözlemişlerdir. Saçan ve arkadaşları ise yaptıkları karşılaştırmalı çalışmada, 0,6 mg/kg roküronyum uygulamış, T2 oluşumundan 15 dakika sonra yaptıkları 4 mg/kg Sugammadex ile 1,7 dakikada, 1 mg/kg Edrophonium ile 5,5 dakikada, 70 mcg/kg Neostigmin ile 17,7 dakikada derlenme izlemişlerdir.
Tüm anestezistlerin korkulu rüyası olan “Entübe edememe, Ventile edememe” senaryolarında da Sugammadex’in çok avantajlı bir molekül olduğu ortaya konmuştur. De Boer ve arkadaşları 1,2 mg/kg roküronyum uyguladıkları hastalara 5 dakika sonra 16 mg/kg sugammadex vermiş ve TOF > 0,9’a ulaşılması 2 dakikadan kısa sürmüştür. Plasebo uygulamalarında ise bu süre 122 dakika olarak ölçülmüştür. Lee ve arkadaşları ise roküronyum + sugammadex birlikteliğini Süksinilkolin ile karşılaştırmıştır. 1,2 mg/kg roküronyum uyguladıkları hastalara 3 dakika sonra 16 mg/kg Sugammadex vermiş, diğer gruptaki hastalar da 1 mg/kg dozunda Süksinilkolin ile relakse edilmiştir. TOF > 0,9’a ulaşılması Roküronyum + Sugammadex grubunda toplam (kürar uygulanma anından itibaren) 6,2 dakika sürmüşken, self-hidrolize bırakılan Süksinilkolin grubunda ise 10,9 dakika sürmüştür. Aradaki bu fark istatistiksel olarak anlamlı bulunmuştur. Ayrıca Sugammadex’in yan etkileri ve kullanım kısıtlılığı ile ilgili renal yetersizlikli hastalarda , Kardiyak problemi olanlarda çalışmalar yapılmaktadır.
Sugammadexin aminosteroid yapılı nöromusküler blokörlerin etkilerini geri çevirmeye yönelik geliştirildiği unutulmamalıdır. Bu nedenle benzilizokinolin grubundan olup, klinik uygulamalarımızda sık olarak kullandığımız atraküryum, cisatraküryum ve mivaküryum gibi ajanlara herhangi bir etkisi yoktur.
Deniz Aytan
Arter Kanülasyonu
Direk radial arter kanülasyonu yoluyla devamlı arteriyal kan basınç monitörizasyonu perioperatif olarak klinisyene hayati bilgiler verir.
Teknik tarihsel olarak 1733 yıllarına dayanır. Cerrahi olarak arteriyel kateterizasyon 20. yüzyılın ilk yarısında tanımlanmıştır.
Anatomik ulaşılabilirliği, kolay kanülasyon ve düşük komplikasyon oranları arteriyal kanülasyon için radial arteri öncelikli bölge haline getirmiştir. Her ne kadar ulnar arter elin beslenmesinde daha dominant arter olsa da anatomik seyri daha derin ve daha kıvrımlı olduğundan kanülasyonu teknik olarak daha zordur.
Bu derlemede elin damarsal anatomisi ve radial arter kanülasyonunun önemi, komplikasyonlar, bunları tedavisi ve arteriyal katater idamesinde heparinli ya da heparinsiz solüsyonların etkinliğinin tartısılması amaçlanmıştır.
Anatomi:
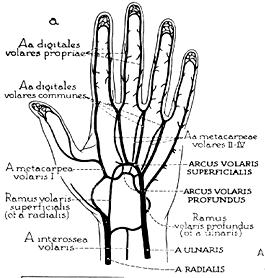
Radial ve ulnar arter ön kol ve elin beslenmesini sağlarlar. Radial arter kubital fossada, biceps tendon medialinde, brakial arterden ayrılır ve radius stiloid çıkıntısına doğru seyreder. Radial arterin çıkış ve seyriyle ilgili %30’lara varan anatomik değişiklikler bildirilmiştir. Ulnar arterde biseps medialinde, kubital fossada ayrılır ve interosseöz arteri vererek psiform kemiğin lateraline doğru seyreder. Ulnar arterin anatomik varyasyonları daha nadirdir (%3-5).
Klasik anatomi literatürü bu iki arter içerisinde radial arterin daha küçük olduğunu, elin beslenmesinde daha az önemli olduğunu bu sebepten radial arter yoksunluğunun unlar arterden daha iyi tolere edildiğini söyler. Bununla birlikte ulnar arter ön kolda çok fazla dal verir, oysa radial arter ön kolda cok dal vermeyerek ele kadar bir arteriyal hat gibi davranır. El elbileği seviyesinde radial ve unlar arterler 4 arktan oluşan ağ yapılanmasıyla arteriyal beslenmeyi sağlarlar. Bu arkların üçü elin palmar yüzeyinde olup palmar karpal ark, derin palmar ark, derin ve yüzeyel palmar arklardır. Dorsal yüz ağ yapısı ise dorsal palmar arktan oluşur. Yüzeyel parmal ark unlar arterin terminal dalı, derin palmar ark ise radial arterin terminal dalı ile oluşur.
Yüzeyel palmar ark komplet ve inkomplet iki tipe ayrılmıştır; bu sınıflama bugün de radial arter yokluğunun tolere edilip edilmemesinde kullanılır. Teorik olarak komplet yüzeyel palmar ark ve derin palmar arka sahip olan hastalar radial ya da unlar arter bağlanmasını tolere edebilirler, çünkü kollateral akım parmakların beslenmesini sağlayabilir. Tersine inkomplet arklı hastalarda radial arter tıkanıklığı dijital iskemi riskini belirgin olarak artırabilir.
Radial Arterde Ateroskleroz Sıklığı: Yaşla beraber intima kalınlığı artmakta, intimal tutulumdan bağımsız olarak da kalsifikasyonlar görülebilmektedir. İleri yaş ve diabet intimal hiperplazi riskini de arttırmaktadır. Radial arter kateterizasyonunun intimada hasar oluşturduğu, segmental ya da diffüz stenoz, hatta arter tıkanıklığına yol açabileceği gösterilmiştir.
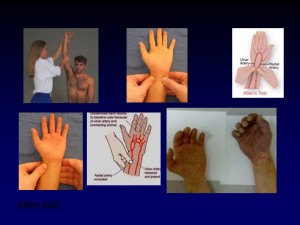
Radial Arter Kanülasyonu Öncesi Elin Beslenmesinin Değerlendirilmesi (Allen Testi): Radial arter kanülasyonu öncesi kollateral akımın yeterliliğinin değerlendirilmesi için Allen testi en çok kullanılan yöntemdir. Radial ve unlar arterlerin her ikisinin de dolaşıma katılıp katılmadığını araştırır. Dirsek eklemi fleksiyonda ve ön kol supinasyonda iken değerlendirilir. Radial ve unlar nabızlar bulunarak her iki baş parmak yerleştirilir. Hasta elini 3 kez açıp kapayarak sıkı yumruk yapar; bu şekilde kanın büyük bölümü boşaltılır; başparmaklar aracılığı ile kompresyon yapılarak hastanın elini açması istenir. Bu aşamada arterlerin basısı nedeniyle el beyaz görülür, nabızlardan biri üzerinden kompresyon kaldırıldığında birkaç saniye içinde elin palmar bölge ve volar palmar yüzleri pembe renk alır. Diğer arter için de test tekrarlanır (ters Allen testi). Anormal Allen test oranı %1-27 arasında bildirilmiştir. Doppler USG eşliğinde yapılan Allen testinin duyarlılığı %100, özgüllüğü %97 olarak gösterilmiştir.
Ulnar Arter Kanülasyonu
Ulnar arterin arteryal basınç monitörizasyonu için kullanımının güvenlik ve etkinlik açısından radial artere benzerliğini gösteren birkaç yayın bulunmaktadır. Bununla birlikte başarısız radial arter kateterizasyonu sonrası ulnar arter kanülasyonu ile dijital iskemi gibi komplikasyonlar bildirilmiştir. Çok sık rastlanmasa da ulnar arter kanülasyonu ile teorik olarak ulnar sinirin nöral travma riski de vardır.
Radial Arter Kanülasyonu Sırasında Gelişebilen Komplikasyonlar: Kanülasyon sonrası komplikasyon oranları %1,5-88 arasında bildirilmiştir. Tıkanıklık, vazospazm, dijital emboli ve iskemi, sepsis, lokal enfeksiyon, psödoanevrizma, hematom, kanama, cilt nekrozu bunlar arasında sayılabilir. Kanülasyon sırasında aşırı extansiyonun medial sinir hasarı yaptığı gösterilmiştir.
Radial Arter Kanülasyonuna Bağlı El iskemisinde Risk Faktörleri: Hastayla ilişkili faktörler inkomplet kollateraller, diğer anatomik varyasyonlar, ateroskleroz varlığı (yaşlılık, diyabet, sigara içiciliği, periferik arter hastalığı), diğer hastalıklar (Raynaud, skleroderma) olarak sıralanır.
Kateter ve yerleştirme tekniği ile ilgili riskler arasında tecrübesiz el, giriş bölgesinde hematom, kanülasyon sırasında oluşan vazospazm varlığı sayılabilir.
Cerrahi ve hastane ilişkili risk faktörleri ise uzamış arteriyal kanülasyon, uzun süreli peroperatif hipotansiyon, uzun süreli ya da yüksek doz vazopressör kullanımı, trombosis veya dijital emboli için yüksek riski olan preoperatif hiperkoagülopatili hastalardır.
Rölatif risk faktörleri olarak girişim sayısının fazla olması, 20G kalınlığından daha kalın kateter, polipropilen kateter (teflona göre), kadın hasta, radial arter çevresinde lokal anestezik maddenin oluşturduğu vazospazm sayılmaktadır.
Daha önceki kanülasyonların sanılanın aksine radial arter oklüzyon riskini arttırmadığı gösterilmiştir.
Arteryal Kateter İdamesinde Heparinli ya da Heparinsiz Yıkama Solüsyonlarının Kullanımı: Devamlı kan basınç monitörizasyonu sırasında arteryal kateterlere uygulanacak ideal solüsyon konusunda farklı görüşler mevcuttur. Bazı merkezlerde heparinize solüsyonlar tercih edilmektedir. Fakat bunların heparinin indüklediği trombositopeniye yol açan antikor oluşumunu hızlandırabileceği de söylenmektedir. Arteryal kateterin idamesinde heparinli ya da heparinsiz solüsyonların karşılaştırılması ile ilgili çeşitli randomize kontrollü çalışmalar mevcuttur. American Association of Critical Care Nurses’ün yaptığı 5139 yoğun bakım hastasını içeren randomize kontrollü bir çalışmada heparinli solüsyonlar heparinsiz olanlara göre üstün bulunmuştur. Optimal heparin konsantrasyonu konusunda da fikir birliği yoktur. İskemik Komplikasyonların Tedavisi: Radial arter kanülasyonu sonrası oluşan iskemik yaralanmaların ideal tedavisi ile ilgili bir görüş birliği bulunmamaktadır. Erken tanı büyük olasılıkla kalıcı hasarı engelleyen en önemli faktördür. Nabız olmaması, arter trasesinin basıklaşması, soluk ve benekli cilt görünümü, gecikmiş kapiller dolum, ağrılı ve soğul el ve parmaklar, motor güçsüzlük gibi belirti ve bulgularda alarme olunmalıdır. Büller ve deri ülserasyonları geç bulgulardır.
Arteriyal akımın değerlendirilmesinde renkli akım doppler USG, anjiyografi ya da MRI kullanılabilir.
Tedavi probleme dönük olmalıdır. Şüpheli trombüs durumlarında trombüsün kateter ucundan aspirasyonu ile arteryal pulzasyonun %60 sağlanabildiği bildirilmiştir. İntraarteryal verapamil, prilokain ve fentolamin iskemik semptomları geri çevirmede etkili olabilir. Diğer önerilen tedaviler düşük molekül ağırlıklı dextran ve düşük doz heparindir. Sınırlı sayıda hastada ürokinaz uygulamasından bahsedilmiştir.
Sıcak uygulama vasospazmı çözebilir. Sempatik sinir blokajı ya da servikodorsal sempatik blok arteryel vazospazmlarda düşünülebilir. İntraarteryal vazodilatatör uygulamanın arteryal spazm tedavisinde güvenilir ve etkin bir yöntem olduğuna dair literatür mevcuttur (örneğin nitrat, kalsiyum kanal blokerleri, lidokain ve molsidomin). Başarısız girişim sonrası radial arter spazmı, ciltaltı nitrogliserinin tek başına ya da % 2 lidokain ile kombine ile uygulaması ile düzeltilebilir.
Cerrahi müdahale kanülasyon sonrası akımın olmadığı ve şiddetli el iskemisinin olduğu hastalarda sıklıkla gerekir.
Dr Filiz Tüzüner