ANESTEZİ YAKLAŞIMI
Aort disseksiyonlu hastada anestezistin sorumlulukları resüsitasyon, hemodinamik stabilizasyon, ağrı tedavisi, TÖE için sedasyon, transfer, anestezi ve perioperatif bakımdır. Ayrıca perioperatif TÖE’da cerrahi kararın verilmesinde de rol oynar.
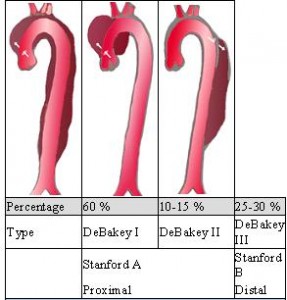
TİP A DİSSEKSİYON:
Monitörizasyon: Bu tip disseksiyonu olan hastalara standart kardiyak anestezik yaklaşım uygulanır. Yeterli periferik venöz damar yolu açılmalıdır. Aşırı sıvı infüzyonu disseksiyonun genişlemesi ve rüptür ile sonuçlanabileceğinden sıvılar titre edilerek verilmelidir. Beta-blokerler ile antihipertansif tedaviye, anestezi indüksiyonu ve idamesinde de devam edilmelidir.
İnnominat arterin disseksiyon ihtimali nedeniyle sağ radyal arter basıncının etkilenmiş olabileceği göz önünde bulundurularak, invazif kan basıncı ölçümü için sol radyal arter kanülüzasyonu tercih edilmelidir. Santral venöz kateterizasyon ise anestezi indüksiyonu öncesi veya sonrasında mutlaka takılmalıdır. Hemodinami, asidoz, koagülopati ve idrar çıkışı yakından izlenip gerekli tedavi uygulanmalıdır. İntraoperatif devamlı TÖE monitorizasyonu cerrahiye yol göstermesi açısından oldukça yararlıdır.
İndüksiyon ve idame: Çıkan aorta cerrahisi sıklıkla medyan sternotomi ile yapılır. İnen aortaya yapılacak herhangi bir müdahale için sol torakotomi gereklidir. Anestezi idamesinde isofluran veya sevofluran gibi miyokard fonksiyonlarını olumlu yönde etkileyen volatil anestezikler ve/veya propofol idamede kullanılır. Optimal cerrahi görüş sahası ve hasta konforu için opioid analjezikler (fentanyl/alfentanil/morphine) ve kas gevşetici ajanların kullanımı uygundur. Postoperatif erken ekstübasyon ve nörolojik muayeneyi geciktirebileceği için kas gevşeticilerin yüksek doz kullanımından kaçınılmalıdır.
Kanülasyon seçenekleri ve kardiyopulmoner bypass: Kardiyopulmoner bypass (KPB) için, disseksiyonun anatomisi ve aciliyetine göre farklı kanülasyon bölgeleri seçilebilir. Anterograd perfüzyon amacıyla arteryel kanülasyon, disseksiyondan etkilenmediyse distal arkus aortadan, sağ subklavien arterden, innominat arterden veya disseke olan çıkan aortanın gerçek lümeninden yapılabilir. Anteregrad perfüzyon için alternatif kanülasyon bölgeleri ise sol ventrikül apeksi ve aort kapağıdır. Retrograd aortik perfüzyon için femoral arter kanülasyonu tercih edilebilir. Venöz kanülasyon ise sıklıkla sağ atrium yoluyla sağlanır. Femoral veya bikaval kanülasyonlar, venöz kanülasyon için diğer seçeneklerdir. TÖE, bütün bu kanülasyon işlemleri sırasında yol göstericidir.
İşlem distal aort anastomozu sırasında parsiyel KPB veya derin hipotermik sirkulatuar arresti (18-20oC) gerektirebilir. KPB ve aortik cross-clamp zamanları cerrahinin zorluğuyla doğru orantılı olarak uzayabilir. Cerrahi tamir sonrası dolaşım gerçek lümene yönlendirilir ve dolaşım tekrar saplanır. Daha sonra KPB sonlandırılır.
Serebral koruma: Arkus aortayı içine alan disseksiyonların cerrahisinde beyine giden kanın kesilmesi gerekir. Bu işlem sırasında oluşabilecek serebral hasarı önlemek amacıyla ya elektriksel aktivitenin durdurdulmasıyla birlikte derin hipotermi veya serebral perfüzyonunun devamını sağlayacak retrograd veya anterograd akımdan yararlanılır. Hastanın kafası dolaşım arresti sırasında buzda tutulmalıdır. Soğutma işlemi sırasında metilprednizolon, tiopental ve lidokain uygulamasının serebral metabolizmayı azaltarak nörolojik hasarı sınırlayabileceği düşünülmektedir. Ayrıca isofluran ve sevofluran gibi volatiller koruyucu etkiler gösterebilirler. Halojenlenmiş volatil ajanların özellikle kalpte olmak üzere diğer organlarda da iskemik hasardan koruyucu (ischaemic preconditioning) etkiler gösterdiği unutulmamalıdır. Furosemid ve mannitol diürezi sağlamak ve sirkülatuar arrest sonrası serbest radikalleri temizlemek üzere kullanılabilir. Cerrahi sırasında nörofizyolojik monitörizasyon tekniklerinden yararlanılması nörolojik defisit riskini azaltabilmekte. Bispektral indeks (BIS) gibi yeni EEG modaliteleri anestezi ve cerrahinin farklı aşamalarında bize beynin durumu hakkında bilgi verebilme avantajını sağlar.
Isı regülasyonu: Sıvıların ve hasta yatağının ısıtılması, ısıtıcı batteniyelerin kullanımı hastanın KPB’tan çıkışında hastayı ısıtmaya yardım eder ve KPB sonrası hipotermiden korur.
Koagülasyon: Major kanamalara, uzamış KPB veya dolaşım arrestine, hipotermiye, masif kan transfüzyonuna veya ilaçlara bağlı olarak dissemine intravasküler koagülopati (DİK) gelişebilir. Bu vakalarda aprotinin (KPB öncesi, sırasında ve sonrasında infüzyon şeklinde) ve traneksamik asitin profilaktik kullanımı önerilmektedir. Tromboelastografi kullanımı, koagülasyon tedavisinin başarısını izlemede yardımcı olur. Kompleks transfüzyon gereksinimleri nedeniyle hastaların hematolog ile konsülte edilmesi yarar sağlayabilir.
Analjezi: Analjezi sıklıkla perioperatif yüksek doz opioid kullanımı ile sağlanır. Epidural analjezi spinal hasara neden olabilme veya spinal hasarı maskeleyebilme riski nedeniyle, bu vakalarda tartışmalıdır.
TİP B DİSSEKSİYON:
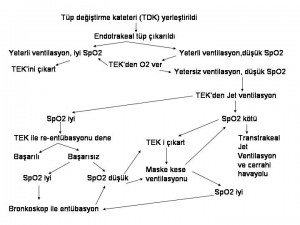
İnen aorta veya torakoabdominal aorta disseksiyonlarına cerrahi olarak yaklaşılacaksa, sol lateral torakotomi gereklidir. Bu vakalarda çift-lümenli endotrakeal tüp ile tek akciğer ventilasyonu standarttır. Sol subklavien arterin klampe edilebilme ihtimali göz önünde bulundurulmalı ve bu nedenle sağ radyal arter monitorizasyonu sağlanmalıdır. Ayrıca alt ekstremitelerin perfüzyonunun yeterli olup olmadığını anlamak amacıyla femoral arter monitorizasyonu da gereklidir.
Spinal kord iskemisi: Cerrahi girişim sırasında aortik klempaj spinal kord iskemisine neden olmaktadır. 30 dakikayı geçen spinal kord iskemisi sonrası nörolojik defisit insidansı ciddi şekilde artmaktadır. Spinal kord koruması amacıyla pek çok farmakolojik (nalokson, metilprednizolon) veya non-farmakolojik yöntem uygulanmaktadır. Girişim sırasında serebrospinal sıvının drenajı, distal aotanın perfüzyonu, epidurak soğutma gibi yöntemler spinal kord koruması için uygulanmakta ve nörolojik defisit insidansını azaltmaktadır.
POSTOPERATİF YAKLAŞIM
Cerrahiden sonra hasta, mutlaka yoğun bakım ünitesinde monitorize şekilde yakın takip altında olmalıdır. Hemodinamik stabilizasyon, ısınma, yeterli gaz değişimi sağlanıp, cerrahi kanama minimal hale gelene dek mekanik ventilasyona devam edilmelidir. Kan basıncı yeterli analjezi ve anti-hipertansif tedavi ile kontrol altında tutulmalıdır. Nörolojik ve periferik dolaşım da dahil olmak üzere hasta, tam bir fizik muayeneden geçirilmelidir. EKG ve akciğer grafisi çekilmelidir. Gereken hastalarda koagülopati ile mücadeleye devam edilmesi ve renal replasman tedavisi uygulanmalıdır. Bu hastalarda postoperatif en sık karşılaşılan problemler, visseral iskemi, metabolik asidoz, infeksiyon ve respiratuar komplikasyonlardır.
Alternatif Girişimler
Tip B disseksiyonlarda, özellikle torakotominin riskli olabileceği veya yandaş hastalıkları olan hastalarda endovasküler yaklaşım düşünülebilir. Bu hastalarda perkütan stentleme ve/veya fenestrasyon açık cerrahiye iyi bir alternatif oluşturmaktadır. Yırtığın bulunduğu segmentin rekonstrüksiyonu, yalancı lümenin tromboze edilmesi, gerçek lümenin yeniden oluşturulması ve aortadan çıkan dallarda akımın sağlanması amaçlanır. Endovasküler girişimler lokal, rejyonal veya genel anestezi altında uygulanabilmektedir. Lokal anestezi ile komplikasyon insidansının genel anesteziye oranla daha düşük olduğu bildirilmektedir. Geniş segmenti içeren endovasküler yaklaşımda spinal kord iskemisi olabileceği dikkate alınmalıdır.
MEDİKAL TEDAVİ
Komplike olmamış inen aorta disseksiyonlarında medikal tedavi tercih edilir. Yeterli analjezi sağlanır. Temel amaç, kan basıncını düşürmek yoluyla disseksiyonun ekstansiyonunu önlemektir.
PROGNOZ
Aort disseksiyonu olan hastalarda, aortik rüptür, kardiyak tamponad, inme ve visseral iskemi en sık ölüm sebepleridir. En son kaynaklara göre, tip A disseksiyonunda cerrahi tedavi gören hastaların mortalitesi %26 iken medikal tedavi görenlerde bu oran %58’dir (ileri yaş ve komorbiditeler nedeniyle). Tip B disseksiyonunda ise mortalite sırasıyla %31,4 ve %10,7’dir. Taburcu olan hastaların kan basıncı kontrol altında tutulmalı ve rutin kontrolleri planlanmalıdır. Tedavi görüp taburcu olmuş hastalarda 10 yıllık mortalite ise % 55’tir.
Miray Kılıç