Postoperatif Analjezide Yeni Ufuklar
Konuşmacılar: Mukadder Orhan Sungur, Tülay Özkan Seyhan
Konuşmacılar: Mukadder Orhan Sungur, Tülay Özkan Seyhan
Anestezistler olarak pek çok tehlikeye açık ortamlarda çalışıyoruz. Enfeksiyon etmenlerine ve kimyasal maddelere maruziyet, yaralanma riski içeren gereçlerin kullanımının yarattığı riskler, anesteziklere bağlı hava kirliliği, non-fizyolojik ışık ve sıcaklık, ciddi boyutlara varan stres günlük hayatımızın parçaları. Ciddi risk oluşturan etmenlerden birisi de radyasyon. Bu kez sizlerde CEACCP’de bu yıl çıkan, iş güvenliği açısından bilmemiz ve dikkat etmemiz gereken noktalara değinen bir yazıyı paylaşmak istiyoruz:
Anestezistler tanı ve tedavide uygulamaları sırasında giderek daha fazla radyasyona maruz kalmaktadırlar. Bu daha çok girişimsel işlemler (ağrı, yoğun bakım, vasküler girişimler) sırasında olmaktadır. Minimal invazif ve daha güvenli müdahalelere doğru yönelimler, anestezinin de içinde bulunduğu birçok branşta floroskopi kullanımında artışa neden olmuştur. Bunlara ek olarak radyoloji hizmetindeki kolaylık servislerde görüntülemenin yaygınlaşmasına, BT taramalarının ve floroskopi esliğinde girişimlerin günün her saatinde yapılabilmesine olanak vermektedir.
Ne yazık ki güvenli iyonizan radyasyon kullanımı ile ilgili eğitim, maruziyetteki artışa paralel olmamıştır. Anestezist işlemi yapanların kendilerini ve hastalarını korumalarına güvenmemelidir. Floroskopiden faydalanılırken anestezist, iyonizan radyasyon kullanımına uygun düzenlemelere uyulduğundan, maruziyetin makul olan en az düzeyde tutulduğundan emin olmalıdır.
Radyobiyoloji
Radyobiyoloji, iyonizan radyasyon fiziğinin canlı dokular üzerindeki biyolojik etkileşimi ile uğraşır. Bu hem terapötik kullanımının hem de zararının temelini oluşturur.
İyonizan radyasyon, enerji vererek geçtiği ortamı etkileyen yüklenmiş partiküllerden oluşur. Lineer enerji transferi (LET) bunu ölçmek için kullanılan terimdir ve ortamın her mikrometresinden (µm) geçen kiloelektrovolt (keV) olarak ölçülür. Radyoterapide kullanılan X ve gama ışınlarının, nükleer füzyonda ortaya çıkan yüksek LET’li α partikulleri ve nötronlara oranla LET’leri düşüktür.
Radyasyon dozu, iki SI birimi ile yani Gray (Gy) ve Sievert (Sv) ile ölçülür. Gray (Gy) birimi, iyonizan radyasyonun absorbe edilen dozudur ve 1 kg madde tarafından absorbe edilen 1 J iyonizan radyasyon olarak tanımlanır. Sievert ise radyasyonun doz eşdeğeri olan birimdir. Dozu tanımlamasına ek olarak Sivert, gama ışını ile karşılaştırıldığında belirli bir radyasyon tipinin iyonizan radyasyonunun biyolojik etkisini de ölçer. 1 Sv, 1Gy’nin bir ağırlık faktörüyle (WR) çarpımına eşittir. X-ışını için bu faktör 1 olduğundan, 1Sv 1 Gy’ye eşittir.
İyonizan radyasyonun doku üzerine etkisi direk ve indirek olabilir. Yüksek LET radyasyonun doku üzerine yaptığı etki direkt etkidir. Atomlar ve moleküllerin direk iyonizasyon veya eksitasyonuna bağlı gelişen fiziksel ve kimyasal olaylar zinciri biyolojik hasara sebep olur. Düşük LET radyasyonun etkisi ise indirektir. Atomlar ve moleküller ile radyasyon arasındaki etkileşim yüksek enerjili elektronlar oluşturur. Bu elektronlar diğer moleküller ile çarpışır ve serbest radikaller oluşur. Serbest radikaller DNA’yı parçalayarak hücrenin kaderini belirleyen biyolojik hasara sebep olurlar. Oluşan serbest radikallerin %80’i (su iyonlari (H2O+) ve hidroksil radikalleri (OH-) gibi) sudan elde edilir. Replikasyonu hızlı olan hücreler bu etkiye en duyarlı olanlardır; ilk etkilenen üreme hücreleri, gastrointestinal ve hemopoetik hücreleri sinir ve kas hücreleri izler.
Biyolojik hasarın klinik yansıması kişiye veya üreme hücrelerine olan etkisine bağlıdır ve maruziyet süresi ile alınan doza göre değişir. Somatik etki bireyin kendisinde oluşan etkileri tanımlar; genetik etki ise gametlerle geçen mutasyonlar sonucu bireyin çocuklarında görülen etkidir. Bu tarz mutasyonlar konjenital malformasyon olasılığını artırırlar ya da düşük veya karsinogeneze neden olan genomik instabilite yaratırlar.
In utero maruziyet genetik etkiden çok somatik olarak kabul edilir. Döllenmeyi takiben ilk haftada iyonizan radyasyon embriyonun ölümüne neden olur. 2-7. haftalar arasındaki organogenez döneminde malformasyon, büyüme geriliği, erken kanser oluşumu gibi etkileri vardır. 8.-40. Haftalar arasındaki fetal evrede ise risk azalmakla beraber benzer etkileri görülebilir.
Somatik etkiler akut ve kronik olabilir. Akut etkiler saatler, günler, haftalar içinde oluşur ve genellikle kısa süreli yüksek doz radyasyona maruziyet sonucu meydana gelir. Kronik etkiler aylar, yıllar içinde belirir ve uzun süre düşük doz radyasyona maruziyet sonucu oluşur. Yüksek dozlar hücre ölümüne neden olma eğilimindedir; çok sayıda hücre etkilenmişse doku ve organ hasarına neden olur. Düşük dozlar ise hücre tamiri veya karsinogenez ile sonuçlanan hücre hasarı oluşturur.
Özellikle yüksek LET radyasyona akut maruz kalınmışsa ortaya çıkan etki, doza ve hücre tiplerinin duyarlılığına göre gelişir. Doz arttıkça hematopoetik sistem üzerindeki etki belirginleşir; kan sayımındaki hafif değişikliklerden immün supresyona, hemoroji ve onarılamaz kemin iliği hasarına kadar değişen şiddette etkiler ortaya çıkabilir. Başlangıçtaki gastrointestinal sistem bozukluğu tam yetersizliğe dönüşür. Çok yüksek dozlarda apne ve kardiyovasküler kollapsla sonuçlanan santral sinir sistemi (SSS) yetersizliği meydana gelir.
Aşağıda alınan doza bağlı akut radyasyon sendromunun değişik klinik tabloları sıralanmıştır:
<0.05 Gy: Etki yok
0.05-0.5 Gy: Kan sayımında değişiklik
0.5-1.5 Gy: Kan sayımında değişiklik, bulantı, kusma, halsizlik, iştah kaybı
1.5-10 Gy: Ani başlayan gastrointestinal semptomlar, kan bileşenlerinde ciddi değişme. (1.5 Gy: ölüm eşiği, çok duyarlı kişiler ölür. 3-5 Gy: Yoğun tıbbi destek olmazsa maruz kalanların %50’si 60 gün içinde ölür. Ölüm nedeni kemik iliği depresyonudur. İyileşme için transplant gerekir.)
10-20 Gy: 2 gün içinde maruz kalanların tümü ölür. Ölüm nedeni gastrointestinal yetersizliktir.
>20 Gy: SSS yetersizliğine bağlı ölüm.
Sıçanlarda X ve gama ışını gibi düşük LET yüksek dozlarda katarakt (2 Gy), cilt yanığı (3 Gy), infertilite (4 Gy), saç dökülmesi ( 5Gy) oluşturabilmektedir. Genel olarak bu tip maruziyetler radyoterapi sırasında oluşur. Ölüme neden olabilen yüksek dozlara maruziyet ise genellikle mesleki kazalar ve yanlışlıkla yüksek doz sonucu olur.
Kronik radyasyon etkileri, fibrozis, atrofi, ülserasyon veya stenoz gibi kronik inflamasyon belirtilerine benzer ve direk maruziyet veya koruyucu üst tabakanın (mukoza ve epidermis) kaybı sonucu oluşur. Ayrıca kanser de (en sık akut veya kronik miyeloid lösemi, cilt, kemik, akciğer, tiroid, meme gibi solid organ tümörleri) oluşturabilir. Toraks filmi için doz 0.02 mSv’dir ve hayat boyu kanser görülme riski 1:1.000.000’dur. Toraks ve batın tomografisi için verilen doz 8-10 mSv’dir ve buna bağlı hayat boyu kanser riski 1:2.000-2.500’dür. Verilen kanser riski oranları 16 yaş altında iki kat artarken, 69 yaşın üzerinde beşte bire düşmektedir.
Sonuç olarak biyolojik hasar, doza bağımlı yani deterministik veya dozdan bağımsız yani stokastik manifestasyonlar olarak ayrılabilir. Doza bağımlı artan hematolojik anormallikler deterministik etkiye örnektir. Çoğunlukla deterministik etkiler için bir eşik değer söz konusudur. Stokastik etkilerin şiddeti ise dozdan bağımsız olmakla beraber dozun artışı olasılıklarını arttırır. Karsinogenez buna bir örnektir. Bu etkilerin görülmesi için aşılması gereken bir eşik değer yoktur; kanser oluşması için neoplastik transformasyona uğrayan bir tek hücre yeterlidir.
Yazının devamında konuyla ilgili düzenlemelere ve güvenlik kurallarına değineceğiz.
Ömür Aksoy’un katkılarıyla hazırlanmıştır.
Anestezİstanbul Kasım Ayı Toplantısı
anestezistanbul 2010-2011-1
Yükleyen nkahraman34. – Bilim ve teknoloji videoları
Kanser gelişmiş ülkelerde 2. ölüm nedeni ve özellikle 4 bölgedeki malign tümörler (akciğer/bronş, kolorektal, göğüs ve prostat kanseri) kansere bağlı ölümlerin yarısından fazlasını meydana getiriyor. Kanserli hastalarin yaklasik yarisinda metastatik hastalik gelisimi ile tani konuyor ve metastatik yuk, hastalikca etkilenmis bolge yerlesimi ve sayisi prognozu belirliyor. Kanser hastalarini hem primer tumorun cikarilmasi hemde tekrarlayan hastaliga yapilan acil mudahalelerin artmasi nedeniyle daha sik ameliyathanelerde goruyoruz. Bunun son 10 yilda kemoterapik (KT) ajan kullanimi ile eslestigini de dusunursek, anestezistlerin bu konuda bilgili olmalari gerekliligi kacinilmaz. Arain’in Current Opinion in Anaesthesiology 2007 de yayinlanan makalesi bu hastalarin akut peroperatif bakimi ile ilgili cok guzel bir derleme. Bu kadar reklam sonrasi makalede bahsedilenler….
Kanser ve metastazin sistemik etkileri:
Agri kanserle iliskili en sik ve en fazla korkulan semptomlardan biri. Yeni tani konulan hastalarin %25’i, ilerlemis kanserde ise hastalarin %75’i agridan muzdarip. Psikolojik stress ve depresyon tum onkoloji hastalarinin %70’inde olculebilir derecede gozlenmektedir ve bunun tedaviyi zorlastirdigi ve prognozu kotulestirdigi dusunulmektedir.
Tum kanser hastalarinin yaklasik yarisinda anoreksi, kilo kaybi, gucsuzluk ve bozulmus immune system ile karakterize kaseksi gelismektedir.
Yine bu hastalarda kemoterapi (KT) ajanlarinin, kan urunlerinin, beslenme desteginin saglanmasi ve tekrarlayan kan testlerinin yapilmasi icin uygun vaskuler girise ihtiyac bulunmaktadir. Santral kateter takilmasi kanserli hastalarda koagulopati, ayni damarlardan tekrarlayan girisimler veya solunum sikintisi olan hastalarda hastanin duz yatamamasi nedeniyle zorlasabilir.
Kanserin kardiak etkileri de klinisyenleri zorlayabilir; aritmiler, radyoterapiye bagli miyokard iskemisi, konjestif kalp yetmezligi, antrasiklin ve radyoterapiye bagli kardiomiyopati, periferik damar hastaliklari ve perikardial hastaliklar gozlenebilir.
Solunum sistemine gelince, KT alan hastalarin %5-10’unda istenmeyen pulmoner reaksiyonlar goruldugu dusunulmektedir. Radyasyon pnomonisi tum isinlanan hastalarin %5-20’sinde gelismektedir. KT sonucu gelisen pulmoner toksisiteye katkida bulundugu dusunulen faktorler arasinda es zamanli oksijen alimi, radyasyon tedavisi ve belirlenmis bir kumulatif esik degerin ustune cikilmasi, varolan solunum problemleri ve ilerlemis yas siralanabilir.
Bu hastalarda gozlenen renal yetmezlik prerenal (atese bagli dehidratasyon veya kalp yetersizligi sonucu yetersiz renal perfuzyon ile), intrensek (sepsis, nefrotoksik ilaclar ile) veya postrenal (yerel ilerlemis pelvik kanser ile uriner obstruksiyon sonucu) olabilir.
Kanser hastalarinda gerek malign gelisim kemik iligi fonksiyonlarini bozdugu, gerekse verilen ajanlar miyelosupresyona neden oldugu icin notropeni yaygindir. Bu durum firsatci infeksiyonlarin ortaya cikisini kolaylastirir, ozellikle nozokomial infeksiyonlar uzamis hastane yatisinin ve mortalitenin onde gelen nedenlerindendir.
Kanser icin kombine KT alan hastalarin %75’inde bulanti ve kusma gozlenir. Bu bulanti ve kusmaya opioidler, anestetik ajanlar, metabolik anormallikler (uremi, hipoksi, ketoasidoz), acil cerrahi sorunlar (ileus veya akut batin) katkida bulunabilir. Yine hiperkalsemi, tum kanser hastalarinin %10’unda gozlenir ve ozellikle akciger squamoz hucreli kanseri, kemik metastazi yapmis meme kanseri, multipl miyelom ile iliskilidir. Hiponatremi ise uygunsuz ADH salinimi sonucunda ortaya cikabilir ve akcigerin kucuk hucreli karsinomu, pankreas kanseri, mesane, prostat, meme ve kolon kanseri ile iliskilidir. Tumor lizis sendromu (TLS) ise tumorun tedavisi esnasinda kullanilan sitotoksik ajanlara baglidir ve hiperurisemi, hiperfosfatemi, hiperkalsemi, ve uremi gibi metabolik bozukluklar ve akut bobrek yetmezligi ile kendini gosterir. TLS ile iliskili tumorler akut veya kronik lemfoid veya miyeloid losemi, akcigerin kucuk hucreli karsinomu, testikuler veya meme kanserleridir.
Hematolojik problemler:
Maligniteye bagli anemi (kronik hastalik anemisi) hastalik ilerledikce derinlesmektedir. Bu hastalarda erotropoetin seviyeleri son derece dusuktur ve eritropoetin ureten hucrelerin ya direkt olarak malignite nedeniyle yada yapilan tedavilerle baskilandigi dusunulmektedir. Lokopeni solid tumorlerin %20 ila 50’sinde gozlenmektedir. Trombositopeni ise genelde KT veya RT ‘ye baglidir. Ayrica splenomegali gelismis hastalarda dalaktaki artmis tutulum nedeniyle gozlenebilir. Kanserli hastalarda tromboz insidansi %2-10 arasindadir ve pek cok trombotik komplikasyon postoperatif gelismektedir. Ozellikle adenokarsinomlu olan hastalar artmis risk altindadir.
Kanser ve Metastazlarin lokal etkileri:
Bas ve boyun kanserlerinde (ozellikle primer akciger kanseri) yuz odemi, pletore, gogus ve boyun venlerinde siskinlik, konjuktival odem, basagrisi, gorme bozukluklari ve suurda degismelerle seyreden superior vena kava sendromu gozlenebilir. Yaygin kanseri bulunan hastalarin %30’unda spinal kord basisi gozlenebilir. Bu hastalarda bel agrisi hemen her zaman norolojik hasardan once yer alir ve varligi klinisyeni MRI taramasi ve gerekirse acil spinal dekompresyon cerrahisi icin uyarmalidir.
Kanser tedavisinin sistemik etkileri:
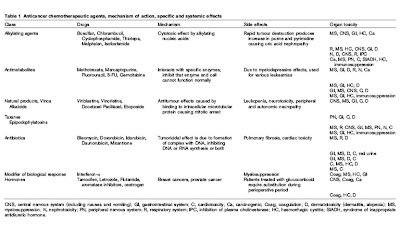
KT ajanlari normal hucrelerde bulunmayan bazi metabolik yolaklari secici olarak bozup malign hucreleri tahrip etmeyi hedeflerler. Bunlarin cogu zaman bulanti, kusma, sac dokulmesi, anoreksi, halsizlik, periferik noropati ve anemi gibi istenmeyen etkileri bulunur. Sistemik KT alan hastalarin %33’unde yasam kalitelerini etkileyen kognitif disfonksiyonlar oldugu dusunulmektedir. Makalede verilen cesitli KT ajanlarinin organ toksiteleri ozetlenmektedir.
Radyoterapi bas ve boyun, serviks, mesane, prostat, deri kanserleri basta olmak uzere uzun sureli kontrol amaciyla pek cok malignitede cerrahinin yerini almaktadir. Ancak istenmeyen yan etkileri arasinda epidermal reaksiyonlar (kuru desequamasyon, artmis pigmentasyon, gec donemde atrofi ve kontraksiyon), akut mukozitler (diare ve gastrit) sayilabilir. Sinir sistemi RT etkilerine cok daha hassastir ve latent periyodu takiben duysal ve motor kayipla seyreden periferik noropati siktir. Akcigerlerde gec donemde (ornegin 2 yada 6 ay sonra) RT’ye bagli fibroz gelisebilir, erken donemde ise akut radyasyon pnomonisi azalmis pulmoner komplians, ilerleyici dispne ve kuru oksuruk ile kendini belli eder. Bobreklerde radyasyon nefropatisi proteinuri, hipertansiyon ve idrar konsantrasyon yeteneginde azalma ile dikkati ceker. ACE inhibitorleri veya ARA bunu iyilestirebilir. Kalpte, radyasyona bagli olarak genelde asemptomatik olan perikardial effuzyonla beraber perikardit (en sik 6 ay- 2 yil sonra) gozlenebilir. Karaciger (KC)de akut fazda 2-6 hafta icinde hepatomegali ve portal hipertansiyon gelisebilir. KC fnk testleri bozulur, kronik fazda ise (6 ay- 1sene) ilerleyici sirotik degisimler gozlenebilir.
Antikanser ilaclar ve anestetiklerle etkilesimleri:
Sitositatik ve anestetik ajanlar beraber verildiginde hucre kulturlerinde tumor gelisiminin engellendigi gosterilmistir. Lidokain bleomisine bagli sittoksiteyi ve DNA hasarini arttirmaktadir. Olasilikla nitrozoksid ve metotreksatin folat metabolizmasi uzerindeki etkisine bagli olarak, N2O kullaniminin metotreksat oldurucu dozunu %50 azalttigi gosterilmistir.
Anestetik ajanlar ve semptomatik tedavi:
Propofol Hodgkin hastaligi nedeniyle gunluk anestezi alan hastalarda 4 haftalik radyoterapi sirasinda guvenle kullanilmistir. Yine sisplatin KT”e bagli bulanti ve kusma tedavisinde propofol etkili olmustur. Bazi kanser hastalarinda engellenemeyen hickiriklar iv midazolam ile kisa surede gecirilmistir.
Kanser Hastalarinda Anestezi:
Preop Degerlendirme:
Dikkat edilecek ve sorgulanacak noktalar:
Intraoperatif Idare:
Temel anestezi monitorizasyonuna ilaveten isi monitorizasyonu ve normoterminin korunmasi rutin olmalidir cunku intraop hipoterminin yara infeksiyonu, olumcul kardiak sorunlar ve artmis kan kaybi ile iliskili oldugu gosterilmistir. Bas, boyun ve mediasten tumorleri olan hastalarda havayolu sorun olabilir, uyanik fiberoptik entubasyon kosullari dusunulmelidir. Bunun gerceklestirilemedigi durumlarda elektif trakeostomi planlanabilir. Havayolu acikligi guvencede olana kadar postop extubasyon planlanmamalidir. Perioperatif kan urunleri tedavisi klinik degerlendirme ile risk ve yararlar goz onune alinarak saglanmalidir. Immun yetmezlikli hastalarda CMV infeksiyonu onemli bir mortalite nedenidir. Ozellikle allojenik kemik iligi ve kok hucre transplantasyonu yapilmis hastalar risk altindadir. Kan profilaktik olarak verilmemeli, risk faktorleri olmayan hastalarda 6-8 gr/dL, risk faktorleri olan hastalarda 10-11 gr/dL hedeflenmelidir. Trombositopenik hastalarda platelet infuzyonlari altin tedavi olsa da, kullanimi ile iliskili infeksiyonlar, platelet refrakterligi bildirilmistir. Benzodiazepinlerin santral sinir sistemi yoluyla immummodulatuar etki gosterdikleri bilinmektedir. Eldeki bazi veriler cerrahi strese karsi sitokin saliniminin benzodiazepin verilmesiyle azaltilabilicegini dusundurmektedir. N2O ve enfluranin klinik konsantrasyonlarinda naturak killer (NK) hucrelerini deprese ettikleri gosterilmistir. Ancak su anda elimizdeki bilgiler bir volatil ajanin digerine ustunlugunu gostermemektedir. Tiopental notrofil kemotaksisini azaltmakta, etomidat ise bazal kortizol salinimini inhibe edip, stres cevabi ortadan kaldirmakta ve yogun bakima yatirilan travma hastalarinda yara infeksiyonu nedenli olumleri arttirmaktadir. Yine intraoperatif yuksek doz fentanil ve morfin kullanimi NK hucrelerini 24 ila 48 saat baskilamaktadir. Henuz elimizde anestezi tekniginin sonuc uzerine etkisini gosteren randomiz kontrollu calismalar yoktur. Ancak deneysel calismalarda Ben-Eliyahu ve arkadaslari meme kanser hucresi injekte edilmis deney hayvanlarinda laparotomi icin rejyonel anestezinin genel anesteziye kiyasla metastazlari azalttigini gozlemistir. Yine yakin zamanda yapilmis bir retrospektif calismada meme kanseri olan hastalarda mastektomi icin paravertebral blok+ genel anestezinin, tek basina genel anesteziye kiyasla 3-4 yil icindeki metastaz yada rekurrens oranini %79 azalttigini gostermistir. Benzer bir retrospektif calisma radikal prostatektomi geciren hastalarda morfin analjezisi+ genel anestezi ile epidural teknik+genel anesteziyi kiyaslamis ve epidural kullanilan grupta kanserin biyokimyasal rekurrensinde (PSA’da yukselme) %65 azalma saptamistir.
Postoperatif Tedavi:
Kronik kanser agrisi cogu zaman akut periop agrinin tedavisini ilac tolerasyonu ve bozulmus agri duyusu nedeniyle zorlastirir. Perioperatif donem boyunca opioidlere devam etmek ve klinik cevaba gore titrasyon önemlidir.