Bundan önceki yazıda sepsisin tanısı, nedenleri, tedavisi yer almıştı. Sepsiste enfeksiyon kaynağının belirlenmesi ve kontrol altına alınması tedavinin önemli bir parçası. Bu hastaların anestezisi de özellik arzetmekte. Yazının bu bölümünde konu “perioperatif” yönetim.
İntraoperatif Yönetim
Enfeksiyonun kontrol altına alınmasına yönelik cerrahi girişimlerin çoğu ameliyathanede ve genel anestezi altında uygulanır. Hastanın bundan optimal yarar görmesi anestezistin primer hedefidir.
İndüksiyondan Önce:
Bu tür girişimlerin çoğu uzun sürdüğünden anestezistin yardıma gereksinimi olacaktır. Hastanın postoperatif dönemde yoğun bakıma gereksinimi olup olmayacağı da önceden düşünülmelidir. Kültüre gidecek materyal, başlanmış olan antibiyoterapiler, tekrar dozlarının zamanlamaları dikkate alınmalıdır. Operasyonun bakteriyemiye ve klinik kötüleşmeye neden olabileceği hesaba katılarak başlanmış tedaviler aksatılmamalıdır.
Standart izleme ek olarak bu tür hastalarda invazif monitörizasyon, belli aralıklarla kan gazı kontrolü, laktat ölçümüyapılması gerektiğinden gerekli ekipmanın hazırlanması gerekmektedir. Eğer işlem sırasında büyük sıvı kayıpları bekleniyorsa yeterli infüzyonun yapılabilmesi için uygun damar yollarının temini uyun olacaktır.
Anestezi İndüksiyonu ve Mekanik Ventilasyonun Başlatılması:
Kaynak kontrol cerrahisi yapılacak hastalarda sepsis, anestezi, intravasküler volüm kaybı, kanama ve cerrahi stres kardiyovasküler instabiliteye neden olurlar. Akciğerlerin denitrojenasyonu için indüksiyona başlamadan önce, yüze iyi oturan bir maske ile 3 dakikaya dek %100 O2 ile solunum yaptırılmalıdır. Bu tür vakaların çoğu acil şartlarında yapıldığından, belki süksinilkolin yerine rokuronyum kullanılarak modifiye hızlı sıralı indüksiyon yapılması gerekebilir.
İndüksiyonda ketamin, etomidat ve yavaş uygulanan propofol kullanılabilir. Çoğu anestezikler vazodilatasyon ve kontraktilitede bozulmaya neden olur. İdeal indüksiyon için klinik cevaba göre anestezikleri titre ederek adım adım ilerlenmelidir. Kullanılan indüksiyon ajanı veya opioidden çok takip önemlidir. Ketamin ve midazolam kısmen hemodinamik stabilite sağlar; kısa etkili fentanil veya alfentanil gibi bir opioid de indüksiyon ajanının dozunda azaltma sağlar. Remifentanil dışındaki opioidlerin etkileri ve etki süreleri bozulmuş hepatik ve renal perfüzyon nedeniyle artabilir. Septik anstabil hastaların indüksiyonunda remifentanil infüzyonunun tek başına veya bir indüksiyon ajanı ile beraber kullanımı önerilmektedir. Bradikardiye neden olmakla beraber, bu hastaların çoğunun taşikardik olduğu ve remifentanilin kontraktiliteye etkisinin minimal olduğu dikkate alınmalıdır. Ayrıca sistemik vasküler rezistansta ani düşmeleri engeller. Tercihan histamin deşarjına neden olmayan bir nöromusküler bloker kullanılarak, kafllı tüple entübasyon sağlanır.
Anesteziklerin ve mekanik ventilasyonun hipotansif etkilerini dengeleyecek volüm resüsitasyonu ve bölünmüş dozlarda yapılacak vazopresörler yarar sağlayabilir. Vazopresör olarak efedrin, fenilefrin veya metaraminol kullanılabilir; herhangibirisinin diğerine üstünlüğü gösterilememiştir. Daha uzun etki için norepinefrin infüzyonu kullanılabilir. Ağır sepsiste mekanik ventilasyonun hedefi yeterli oksijenasyonu (PaO2 >12 kPa *) sağlayacak derecede yüksek FiO2 kullanılmasıdır. Eldeki veriler düşük tidal volüm kullanımını desteklemektedir; böylece pozitif basınçlı ventilasyonun hem akciğerde yarattığı hasar, hem de venöz dönüş ve kalp debisi üzerine olumsuz etkisi azaltılabilmektedir. Yüksek basınç veya volümler akciğer hasarını arttırdığından, oksijenasyon yeterli ise “permissif hiperkapni”ye (PaCO2 >8–9 kPa *) izin verilebilir. Bu değerlerin 3-4 günden fazla tolere edilebildiği ve göreceli olarak güvenli olduğu görülmektedir.
Anestezinin İdamesi:
Anestezide inhalasyon veya iv anestezi kullanımının sürviye etkisi ile ilgili herhangi bir kanıt yoktur. Seçenekler arasında inhalasyon ajanları, iv ajanlar ve opioidler, örneğin remifentanil infüzyonu 0.25-0.5 mikrogr/kg/dak bulunmaktadır. Yöntem hastanın durumuna ve anestezisitin deneyimine göre seçilmelidir. Ağır sepsiste inhalasyon ajanlarının MAC değeri düşer. Ciddi akciğer disfoksiyonunda, inhalasyona oranla iv ajanlarla beyinde stabil anestezik konsantrasyonunun sağlanması daha güvenlidir. Hangi yöntem kullanılırsa kullanılsın anestezi derinliğ bispektral indeks monitörü ile izlenebilir.
Cerrahi sırasında kan kaybı, bakteri veya endotoksin salınımı hemodinamiyi daha da bozabilir. Ciddi kan kaybında kan ürünlerinin kullanımında geç kalınmamalıdır. Volüm resüsitasyonu da sürdürülmelidir. Başlangıç tedavisinde hedeflenen CVP=8-12 cm H2O olmakla beraber cerrahi sırasında intratorasik ve intraabdominal basınçların artışına bağlı olarak yükselebilir. CVP veya PAOP gibi basınçlara oranla, nabız basınç değişkenliği (pulse pressure variation), atım volümü değişkenliği (stroke volume variation) gibi dinamik belirteçlerin volüme cevaplılığı daha iyi öngördüğü gösterilmiştir. Dinamik belirteçler sinüs ritmindeki, kontrole mekanik ventilasyon uygulanan hastada intraoperatif volüm tedavisini yönetmek için kullanılabilir. Eş zamanlı transösofageal ekokardiyografi veya ösofageal Doppler atım volümü değişkenliğini saptamada kullanılabilir. Kalp debisini ölçmek için bir çok alet bulunmaktadır; ölçüm sürekli (pulmoner arter kateteri, ösofageal Doppler, impedans pletismografisi) veya belli aralıklarla (transtorasik veya transösofageal ekokardiyografi, mikst venöz O2 satürasyonu ölçümleri) yapılabilir. Girişim boyunca kardiyovasküler parametreler (kalp hızı, kardiyak dolum basınçları, inotropik durum, sistemik arteryal basınç) belli kalp debisi veya kan basıncı değerlerini hedeflemekten çok, dokuya oksijen sunumunu optimize etmeye yönelik olmalıdır. Serum laktat düzeyi <2 mmol/L ve mikst venöz O2 satürasyonu > %70 global oksijen sunumunun yeterli olduğunu işaret eder.
Oksijenasyon artmış kapiller geçirgenliğe bağlı ortaya çıkan nonkardiyojenik pulmoner ödem oksijenasyonu bozabilir. Hipoksemiyi düzelmek için FiO2 arttırılabilir ve PEEP aşamalı olarak yükseltilebilir. SaO2 en az %90 olana dek FiO2 yükseltilebilir. Buna rağmen hipoksi sürüyorsa hemodinamisi stabil hastalarda PEEP dikkatli bir şekilde arttırılır. Özellikle intrakranyal basıncı yüksek, kompanse metabolik asidozu olan veya ilerlemiş gebeliği olan hastalarda hiperkarbiden kaçınılmalıdır.Bunun dışındaki vakalarda hiperkarbi iyi tolere edilir; hatta permissif hiperkapninin koruyucu etkileri olduğuna dair kanıtlar ortaya konmuştur.
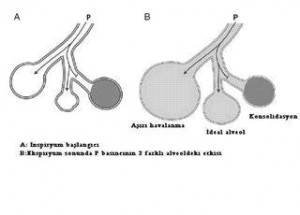
Mekanik ventilasyonda akciğeri koruyucu stratejiler önerilmektedir. İnspiryum sonunda alveol içi ve dışı arasındaki basınç farkı transpulmoner basınç olarak tanımlanır. Plato havayolu basıncı (inspiryum sonunda solunumu durdurmak sureti ile volüm kontrollü mekanik ventilasyon sırasında ölçülür) alveol içine uygulanan maksimal basıncın göstergesidir. Alveol dışı basınç direkt olarak ölçülemekle beraber klinikte plevral basınçtaki değişikliklerin değerlendirilmesi ile tahmin edilebilir. Ekstra-alveolar veya plevral basınç hastanın Trendelenburg pozisyonuna alınmasıyla veya laparoskopide insuflasyona bağlı intra-abdominal basıncın arttırılmasıyla ani olarak yükselir. Plevral basınç yükselirken plato basıncı sabit kalırsa pulmoner gaz değişimi bozulabilir. Öte yandan yüksek transpulmoner basınçlar akciğer hasarı yaratırlar. Erken akut akciğer hasarı (ALI) olan hastalarda ventilasyon stratejisinin hedefi transpulmoner hava yolu basıncında düşme (20-25 cm H2O ile beraber alveolar ventilasyonda azalma) ve abartılı transpulmoner basınçlar (25-30 cm H2O ile beraber barotravma riski) arasındaki uygun dengeyi sağlamak olmalıdır. Kollabe alveolleri açmak (recruitment) için kısa süreli 30-40 mmHg tepe hava yolu basıncı sağlayacak şekilde manuel ventilasyon uygulamak şantı azaltıp intraoperatif bozulmuş oksijenasyonu düzeltebilir. Pnömotoraks riski olan amfizematöz büllü veya ağır kronik obstrüktif akciğer hastalığı olanlarda bu manevra çok dikkatli uygulanmalıdır. Girişim sırasında arteryal kan gazı, tam kan sayımı, koagülasyon profili, elektrolitler, laktat ve glukoz takip edilmelidir. Trombosit ve koagülasyon faktörlerinin fonksiyonunda azalmaya neden olacağından hipotermiye izin verilmemelidir.
Septik Hastalarda Rejyonal Anestezi ve Sinir Bloklarının Rolü:
Hasta bazında periferik blokların stres yanıtı azaltıcı etkisi ve sistemik opioid kullanımının devreden çıkması kar-zarar dengesi açısından değerlendirilerek uygulanabilir. Ancak koagülopati, enfeksiyonun lokal veya sistemik yayılımı ve lokal anesteziklerin asidotik enfeksiyon ortamında etkinliklerini kaybetmeleri gibi faktörler rejyonal tekniklerin kullanımını sınırlamaktadır. Nöroaksiyal teknikler sepsise bağlı hemodinamik problemler göz önüne alınarak dikkatle uygulanmalıdır. Uygulamadan hemen önce yapılmış koagülasyon testlerinin normal olması şarttır. Eldeki verilere göre epidural anestezi kalıcı nörolojik sekel açısından düşük risk taşımakla beraber septik hastalarda ciddi komplikasyon riskinin artmış olduğu hesaba katılmalıdır.
Cerrahi Girişimin Sonlanması:
Batının veya toraksın kapanmasını kolaylaştırmak için bu aşamada ek nöromusküler dozları gerekebilir. Kanama varsa minimal hale gelmesi sağlanmalıdır. Ek doz antimikrobiyal ajanların uygulanması gerekebilir. Tekrar operasyonu gerektirecek olanlarla, ağır hastalarda analjezi, sedasyon ve mekanik ventilasyon postoperatif dönemde sürdürülmelidir. Yoğun bakıma transport güvenli şartlarda yapılmalıdır. Hasta yoğun bakım ekibine ayrıntılı şekilde devredilmelidir.
Ağır Sepsiste Postoperatif Yönetim
Yoğun bakıma giriş APACHE skoru için resüsitasyon öncesi ölçümler değerlendirmeye alınmalıdır. Vazopresörler intravasküler volüm ve uygulanacak mekanik ventilatör stratejilerine göre ayarlanmalıdır. Mekanik ventilasyona bağlı volutravma ve barotravmayı en aza indirecek ventilasyon değerleri ayarlanmalıdır. Düşük basınç, yüksek FiO2 ve uygun alarm limitlerinin ayarlanması uygun olacaktır. En çok 6 ml/kg kadar tidal volüm ve permisif hiperkapni ile pH 7.20’nin altına inmeyecek şekilde solunum desteği verilebilir. Basınç kontrollü veya volüm kontrollü modlar kullanılabilir. Parankim hasarını önlemek üzere, volüm kontrollü moda respiratuar siklus endinspiratuar “pause” içerdiğinde ulaşılan transpulmoner basınç (plato basıncı-plevral basınç) limiti 25-30 cmH2O olmalıdır. Yüksek PEEP (10-15 cm H2O) kullanımı ortaya çıkacak hemodinamik instabilite nedeniyle sınırlıdır. SpO2 %93-95 hedeflenerek FiO2 %60’a düşürülebilir.
Antimikrobiyal tedaviye devam edilmelidir. Kullanılan ajanlar mikrobiyoloji sonuçlarına göre günlük değerlendirilmeli, etkinlik sağlanırken rezistans ve toksisite engellenmelidir. Tedavi 7-10 günle sınırlandırılmalıdır.
Akut miyokard enfarktüsü ve anstabil anginası olanlar dışında, restriktif transfüzyon stratejisi uygulanan vakalarda (Hb > 7 g/dl ise transfüzyondan kaçınılması) mortalitenin daha düşük olduğu gösterilmiştir. Koagülasyon testlerindeki anormallikleri düzelmek için taze donmuş plazma kullanımına sadece klinik olarak kanaması olan veya invazif girişim planlanan hastalarda başvurulmalıdır. Trombosit transfüzyonu sadece, kanamaya bakılmaksızın trombosit sayısı ≤ 5000/mm3 olan veya 5000-30.000/mm3 olup belirgin kanama riski olan hastalarda yapılmalıdır.
Derin ven trombozu profilaksisi genellikle koagülopati ile ilgili şüpheler kalktığında gündeme gelmektedir. Ölüm riskinin yüksek olduğu (APACHE skoru >25 veya çoklu organ yetmezliği) sepsise bağlı organ disfonksiyonu olan hastalarda, eğer kontrendikasyon yoksa, rekombinan human aktive protein C (recombinant human activated protein C, rhAPC) kullanılması düşünülebilir. Ağır sepsisli erişkin ve ölüm riski düşük hastalarda (APACHE II < 20 veya tek organ yetmezliği) rhAPC kullanılmamalıdır.
Glisemik kontrolün devamı (<8.5 mmol/L **) septik sürecin kontrol altına alınmasında önemlidir. Geniş bir randomize internasyonal seride sıkı (4-6 mmol/L **) ve liberal (6-10 mmol/L **) glukoz kontrolü yapılan hastalar arasında mortalite veya ortalama organ yetmezliği skorunda fark bulunmamıştır. Ancak yoğun tedavi gören grupta ağır hipoglisemi (≤ 2.2 mmol/L **) sıklığı ve istenmeyen etkiler ciddi oranda daha fazla görülmüştür. Bu nedenle ağır sepsisli hastalarda kan şekeri 6-10 mmol/L ** düzeyinde tutulmalıdır.
Beslenme ağır sepsiste önemli bir bileşendir. Nazogastrik tüple enteral beslenme enterosit integritesini koruma ve beslemek için en iyi seçimdir. Gastrointestinal koruyucu önlemler (stres ülser profilaksisi) ve antiemetikler de kullanılmalıdır. Total parenteral nutrisyon (TPN) cerrahi kontrendikasyon varlığında veya enteral yolun tüm gereksinimi karşılamadığı vakalarda gündeme gelmelidir. Perioperatif dönemde TPN veya enteral beslenme kesildiğinde hastalarda hızla hipoglisemi gelişebilir.
Sıvı ve vazopresörlere yeterli cevabın alınamadığı hipotansiyonda iv hidrokortizon kullanımı düşünülebilir. 7 günlük düşük doz hidrokortizon ve fludrokortizon tedavisinin septik şok ve rölatif adrenal yetmezlik olan hastalarda yan etkileri arttırmadan mortaliteyi azalttığı gösterilmiştir. Yoğun bakımda septik şok vakalarında, günlük dört doza bölünmüş toplam 200 mg veya sürekli infüzyon halinde toplam günlük 240 mg hidrokortizon önerilmektedir. İntraoperatif dönemde düşük doz steroid uygulamasının hemodinamik stabilite sağlamada rolü bilinmemektedir. Ağır sepsiste glukokortikoidlerin tedavideki rolünün daha fazla araştırılması gerekmektedir.
Ağır sepsisli hastaların %23’ünde akut renal yetersizlik gelişmektedir. Renal replasman tedavisi asidozu, hiperkalemi veya sıvı yükünü düzeltmek için başlatılabilir ve akut tubuler nekroz düzelene dek sürdürülebilir. pH< 7.1 olmadıkça sodyum bikarbonat önerilmemektedir. Sürekli veno-venöz hemofiltrasyon ile aralıklı hemodiyaliz arasında survi açısından fark saptanamamıştır. Ancak hemodinamik instabil hastalarda sürekli renal replasman daha pratik olabilir.
Analjezi ve sedasyon infüzyon halinde sürdürülmelidir; ancak ağır sedasyon ve nöromusküler blokaj önerilmemektedir.
Sonuç olarak ağır sepsis ciddi bir sağlık problemidir. Genellikle enfeksiyon kaynağının kontrol altına alınması için cerrahiye gerek duyulur. Anestezistin bu vakalarda rolü belirleyicidir. Zamanında sıvı resüsitasyonunun başlanması, hemodinamik destek, etkin antimikrobiyal tedavi stratejileri surviyi arttırmakta önemli rol oynayacaktır. Konunun daha pek çok çalışmayı gerektirdiği de açıktır.
* 1 kPa = 7.5 mmHg
** mg/dl = 18 x mmol/dl