Bu bölümde KH için şimdiye dek uygulanmış yöntem ve ilaçlara değineceğiz.
Fizyolojik Yöntemler
Operasyon bölgesinde kan basıncının düşürülmesi ile kanamanın azaltılmasında fizyolojik mekanizmalar kullanılabilir.
Operasyon bölgesinin kalp seviyesinden yukarıda tutulması bu alandaki kan basıncını azaltır, venöz basıncı düşürür. Ancak bu teknikte hava embolisi riski mevcuttur.
Mekanik ventilasyonun etkilerinden de yararlanılmıştır. Hiperventilasyon hipokapniye bağlı vazokonstriksiyon sağlayarak kan akımını azaltır. Hipoventilasyon ise hiperkapniye bağlı vazodilatasyon ile kan akımını arttırır.
Farmakolojik Ajanlar
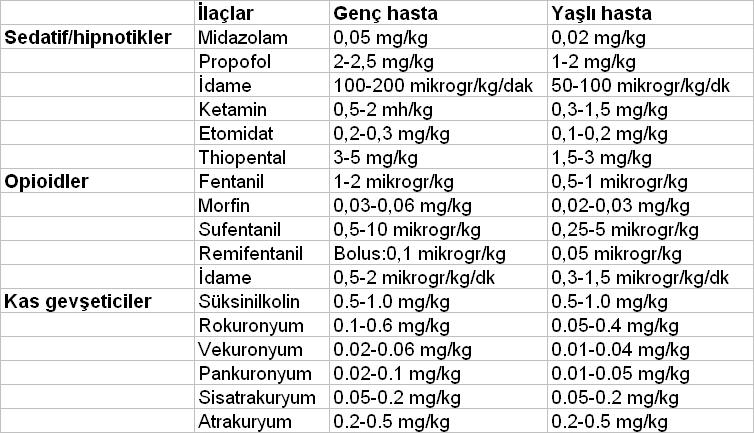
KH için ideal ajan kolay uygulanabilmeli, etki hızlı başlamalı ve kısa süreli olmalı, sonlandırıldığında etkisi kısa sürede kaybolmalıdır. Toksik metabolitleri olmamalı, vücuttan hızlı atılabilmeli, vital organlara ciddi etkileri olmamalı, etki doza bağımlı ve tahmin edilebilir olmalıdır. Ne yazık ki ideal tanımına uyan bir ajan henüz elimizde yoktur.
KH için kullanılabilecek ilaçlar şöyle sınıflandırılabilir:
a.Tek başına başarılı bir şekilde kullanılan primer ajanlar; örneğin inhalasyon anestezikleri, nitroprussid, nitrogliserin, trimetafan, alprostadil (prostaglandin E1), adenozin, remifentanil ve spinal anestezi
b.Tek başına veya diğer ajanların istenmeyen yan etkilerini azaltmak amacıyla ek olarak kullanılanlar; örneğin kalsiyum kanal antagonistleri (örnek nikardipin), beta-blokerler (propranolol, esmolol), fenoldopam
c.Sadece primer ajanlarla birlikte kullanılabilen sekonder ajanlar; örneğin ACE inhibitorleri, klonidin.
Epidural ve Spinal Anestezi
Epidural ve spinal anestezi, kan basıncını ve kanamayı azaltmaları dolasıyla, şimdiye kadar KH için iyi teknikler olarak gösterildi. Spinal anestezinin sempatik liflerde neden olduğu blokaj, periferik vasküler direnci ve venöz dönüşü azaltarak kardiyak debiyi düşürür. Ancak ilaç dozuyla ilacın etkisi arasında ilişki olmaması, blok seviyesiyle öngörülemeyen ve kontrol edilemeyen hipotansiyonun derecesi ve etki süresinin çok değişken olması dezavantajlarıdır. Hipotansiyon hedeflenen minimal alt sınırı aşabilir ve hipotansiyonun kontrolü için vasopressör gerekebilir. Ayrıca bu teknik abdominal cerrahi ve alt ekstremite cerrahisi ile sınırlıdır.
Turnike ile spinal anestezi veya turnike olmadan epidural anestezi ile yapılan diz ameliyatlarında kanamayı azaltmada aynı sonuçlara ulaşılmış. Kanamanın, kalça cerrahisinde spinal anestezi ile epidural anesteziye göre daha fazla olduğu, spinal anestezi ile yapılanlarda D-dimer düzeyinde yükselme ve trombin zamanında düşüş olduğu bildirilmiştir. Ancak hiç renal, nörolojik veya kardiyopulmoner komplikasyonlar belirtilmemiştirdi. Epidural anestezinin sol ventrikül disfonksiyonu olan hastalarda dahi güvenle kullanılabildiği, intraoperatif kan kaybının propofol+ remifentanil ile TIVA uygulamasına oranla daha az olduğu gösterilmiştir.
İnhalasyon Anestezikleri
Halotan ve enfluranın tersine isofluran düşük konsantrasyonlarda, intrakranyal basıncı arttırmadan kan basıncını düşürür. Daha yüksek konsantrasyonlarda her ajan, serebral kan akımında artış ve serebral otoregülasyonda bozulmadan sorumlu vazodilatör etkiyi indükler. 1 MAC’lık konsantrasyon vasküler kompliyansta düşüşle birlikte intrakranyal basınçta artışa yol açabilir. Refleks taşikardi ve postoperatif rebound hipertansiyon barorefleks kontrol mekanizmasının ve inhibisyonunun eksik olmasının ve anasteziklerle sempatik stimülasyonun sonuçlarıdır.
Yüksek konsantrasyondaki inhalasyon anestezikleri spinal ve serebral cerrahi sırasında kullanılan uyarılmış potansiyalleri (evoked potential) deprese eder. Bu nedenle KH için inhalasyon anesteziklerinin tek başına kullanımı tavsiye edilmemektedir. Sevofluranın yüksek konsantrasyonlarda koroner vazodilator özelliklere sahip olduğunu da gösterilmiştir.
İnhalasyon anestezikleri güvenli klinik konsantrasyonlarda sadece hafif hipotansiyon oluşturmakta, gerçek anlamda KH için adjuvan hipotansif ajanlara gerek duyulmaktadır.
Opioidler
Analjezik etkileri için anestezide kullanılan bazı opiodler istenmeyen hipotansiyonu provoke edebilmektedir. Bu etkileri nedeniyle KH için diğer hipotansif ajanlara ek olarak kullanılmışlardır. Ancak remifentanil çıkana kadar, uzun yarılanma ömürleri nedeniyle opioidlerin KH için kullanımı güçtü.
Remifentanilin kan basıncını istenilen seviyeye düşürdüğü, orta kulak kan akımını azalttığı, metabolik komplikasyonlar ve kulak mikrosirkülasyonunun otoregülasyonunda bozulma olmadan kansız bir operasyon sahası sağladığı gösterilmiştir. Remifentanilin hipotansif etkisi ve kısa yarılanma ömründen yararlanarak, propofol veya sevofluran ile kombine edildiğinde, orta kulak cerrahisinde, muhtemel sempatik sinir blokaj mekanizması ile, nitroprussid veya esmololün yerine KH sağlanabilir. Fonksiyonel endoskopik sinus cerrahisinde propofol ile kombine edildiğinde, alfentanil+isofluran veya sufentanil+sevofluran veya fentanil+ izofluran kombinasyonundan daha iyi cerrahi görüş sağlamıştır.
Güncel literatür ışığında, inhalasyon anesteziği veya propofol ile kombine edildiğinde remifentanil, kar zarar oranına göre en iyi KH sağlayan ajandır; çünkü standart anestezi tekniğine göre, kanamayı ve transfüzyonu azaltmak için potent bir hipotansif ajan eklenmesine gerekli kalmamaktadır.
Vazodilatörler
Sodyum Nitroprussid: 1950’den beri en sık kullanılan hipotansif ajan olmuş ve hep referans ajan olarak kullanılmıştır. Doğrudan periferik vazodilatör etkisi vardır, direnç damarlarını gevşetip venöz dilatasyona ve venöz dönüşte azalmaya sebep olur; sekonder olarak arteryel dilatasyon yapar. Etki başlangıcı çok hızlıdır (<30 sn) ve ilacın kesilmesinden sonra hipotansif etkisi 2 dakikadan fazla sürmez. Ancak taşiflaksi, rebound hipertansiyon, miyokard iskemisi, kafa içi basınç artışı, artmış intrapulmoner şant, trombosit disfonksiyonu ve siyanid toksisitesi gibi birçok dezavantajı da vardır. Periferik vazodilatasyon, baroreseptör uyarımlı refleks taşikardi ve miyokard kasılmasında artışa sebep olur. Sempatik sistem ve renin-anjiotensin sisteminin aktivasyonuna bağlı kardiyak debi artışına neden olur. Plazma katekolamin seviyesi ve renin aktivitesi artışı nitroprussid infüzyonu kesilmesinden sonra rebound hipertansiyondan sorumludur.
Nitroprussid toksisitesi yıkım ürünleri olan serbest siyanid ve tiyosiyanidin plazmada birikmesine bağlıdır. Bu toksinlerin konsantrasyonu kullanılan total dozla orantılıdır. Siyanid metabolizması karaciğerde olur ve oluşan tiyosiyanid, böbrek yoluyla atılır. Tiyosiyanide dönüşüm yavaş olursa, siyanid konsantrasyonu hipoksiyi ve metabolik asidozu indükleyecek kadar yükselebilir. Bu, karaciğer hasarlı kişilerde bir risktir. Tiyosiyanid toksisitesi, uzun veya yüksek doz kullanımda veya böbrek hastalarında görülebilir. 100 mg/L tiyosiyanid plasma konsantrasyonunda görülen toksisite semptomları kas ağrısı, mental konfüzyon ve bulantıdır. Taşiflaksi, daha yüksek doz kullanımına sebep olmuş ve anoksik olaylar gelişmiştir; şans eseri bu olaylar geri dönüşlü olduğu için ölümcül olmamıştır. Taşiflaksinin kompleks yapısı açıklanamadığından, toksisiteyi önlemek doza dikkat edilmelidir. Önerilen maksimum doz 8 micg/kg/dak idame dozudur; günde 2 µg/kg/dak aşılmamalıdır.
Tanımlanan dezavantajlar sonucunda, premedikasyon için nitroprussid, propranolol veya kaptopril ile kombine edilir; bu kombinasyonlar, KH elde etmek ve rebound hipertansiyondan kaçınmak için gerekli nitroprussid miktarını %70’ten fazla düşürmüştür. Toksisite çalışmaları nitroprussidin, T lenfosit ve interlokin 6 aktivasyonundan, postop spontan adrenerjik orijinli trombosit agregasyonundan,dalak perfüzyonunda düşüşten ve belli derecede hepatik sitolizden sorumlu olduğunu göstermiştir. Nitroprussid ile diltiazem kombinasyonu, operasyonda kanamayı azaltırken, sadece nitroprussid ile tedavi edilen hastalardan oluşan pilot çalışmalarda görülen solunum sıklığı artışıyla, tiyosiyanidlerle ve kardiyak debiyle ilgili dezavantajları azaltmıştır. Premedikasyon için nitroprussid ve enalaprilat kombinasyonu, kan basıncını istenen seviyeye indirirken nitroprussid dozunu belirgin olarak azaltır.
Endoskopik sinus cerrahisinde, timpanoplastide cerrahi görüş kalitesini arttırmıştır; fakat hiperkapni ve laktik asidozu provoke etmiştir. Prostatektomide hemodilüsyon veya plaseboya oranla kan kaybını daha çok azaltmış ve toplam maliyeti %40 düşürmüştür.
KH için uygulanırken taşiflaksiye bağlı yan etkileri, arteryel basıncı ve metabolik sorunları yakından takip etmek gereklidir. Bir referans ajan olarak kullanılsa da, KH’un kar/zarar oranını geliştiren standart anesteziye dayanan efektif teknikler bunun yerine kullanılabilir.
Nitrogliserin: Nitrogliserinin venöz kapasitans damarlarına ve ikincil olarak arterlere nonspesifik, direkt vazodilatör etkisi vardır. Yarılanma ömrü kısadır, klinik toksik metaboliti yoktur. Venöz kan volümünü arttırır, venöz dönüşü azaltır; kardiyak debi bu oranda azalır. Bu fenomenden kaynaklanan arteryel vasokonstriksiyonu sınırlayan anestezik ajanlarla, adrenerjik yanıt kısmen bloke edilir. Nitroprussid ile karşılaştırıldığında nitrogliserin, hipotansiyonu indüklemede o kadar etkili değildir; daha yavaş etki eder. Rebound hipertansiyona veya miyokard iskemisine yol açmaz. Bununla birlikte nitrogliserin, nitroprussid ile karşılaştırıldığında taşikardi, serebral kan akımı ve intrapulmoner şantta artışa sebep olur. Kan basıncındaki düşüş total kan volümüne bağlı olduğundan, düşük kan hacmine sahip hastalarda kan basıncında aşırı düşüş olup koroner kan akımı bozulabilir. 5 mg/kg’dan fazla miktarda nitrogliserin methemoglobinemi yapabilir. Trombosit agregasyon azalması nitroprussidden daha azdır ve hemostazı değiştirmez. Çalışmalar yalnız veya beta bloker ile kombine kullanıldığında transfüzyon ihtiyacını azalttığını göstermiştir. Sevofluranla kullanıldığında sevofluran dozunu azaltarak hepatik toksisite riskini azaltsa da, mandibuler cerrahide kanamayı azaltmada nitrogliserin, izoflurandan daha az etkilidir.
Özet olarak, nitrogliserin kanamayı azaltmada nitroprussid gibi diğer vazodilatörlere bir üstünlük gösterememiştir ve nitroprussidden daha iyi bir kar/zarar oranı olsa da, monitorizasyonu gerektirir. Remifentanil ile standart bir hipotansif anestezi tekniği, böyle bir protokole ihtiyaç duymaz.
Adenozin: Pürinlerden türetilen doğal bir madde olan adenozin, adenozin trifosfatın iv verilmesinden sonra metabolize edilmesi sonucunda oluşur; daha ileri metabolizma ürik asit oluşumuyla sonuçlanır. Adenozin, doza bağımlı sistemik ve koroner arteryel vazodilatasyona sebep olur. Plazma renin aktivitesi ve katekolamin seviyeleri artar. Serebral kan akımını arttırır, serebral mikrovasküler sirkülasyonun otoregülasyon fonksiyonunda bozulmaya sebep olur. Adenozinin plazma yarılanma ömrü sadece 10-20 saniyedir ve santral venöz kateterden verildiğinde daha kullanışlıdır. Hızlı degrade olduğundan, yüksek dozları gerektirir. Ancak bu fenomen, adenozinin degradasyonunu inhibe eden dipiridamolün eklenmesiyle engellenebilir. Adenozin, taşiflaksi, rebound hipertansiyon veya taşikardi yapmasa da, intrakardiak iletiyi yavaşlatır ve predispozan kişilerde miyokardiyal iskemiye eğilimi arttırır. Çalışmalar, glomerüler filtrasyonda ve renal kan akımında azalmayla sonuçlanan preglomerüler damarlarda vasokonstrüktif etkiyi vurgulamıştır; bu, selektif adenozin A1 reseptör antagonisti ile premedikasyonuyla önlenebilir. Bronşial spazm da tanımlanmıştır ve varsayılan mekanizmalar şunları içerir: adenozinin bronş düz kaslarına direkt etkisi, mast hücrelerinden histamin salınımı, kolinerjik stimulasyon, adenozin reseptörlerinin uyarılması ve intraselüler c-AMP seviyesinin değişimi. Adenozin, gerekli dozu ve yan etkileri azaltmak için dipiridamole ihtiyaç duyan pahalı bir üründür. İhtiyaç duyulan dozu azaltan sinir bloğu ve isofluranla kombine kullanılarak mandibuler cerrahide kan kaybını düşürdüğü bildirilmiştir.
Diğer vazodilatörlerle karşılaştırıldığında adenozinin kar/zarar oranı en iyilerden biri değildir; örneğin hipotansif spinal veya hipotansif remifentanil anestesizinden daha düşüktür.
Alprostadil: Alprostadil, vasküler direnci azaltarak arteryel basıncı düşüren doğal bir maddedir. Bir dizi etkisi vardır: trombosit agregasyonunun inhibisyonu, immun yanıta etki, antiinflamatuar etki, faktör X’un stimülasyonu. İntrensek negatif kronotropik etkisi vardır ve diğer vazodilatörlerde görülen refleks taşikardiyi sınırlandırır. Devamlı infüzyon olarak verilebilmesine imkan sağlayacak şekilde çok hızlı metabolize olur; ilacın %70’i akciğerde ilk geçişte elimine olur, metabolitler böbrekten atılır. Alprostadil, küçük renal arterleri dilate ederek glomerüler filtrasyonu arttırır, atılımını ve diürezi arttırır. Alprostadilin serebral kan akımı ve serebral damarların otoregülasyonu üzerine yan etkisinin olmaması, bu ilacın nöroşirurji ve kardiyak cerrahide kullanılmasına sebep olmuştur.
Alprostadilin yan etkileri, apneye sebep olan solunum depresyonu, bronşial konstriksiyon, bradikardi, abdominal ağrı, diare ve hipertermidir. Bir kalça cerrahisi çalışmasında hemodilüsyonla kombine olarak uzun süreli (>120 dak) alprostadil kullanımının, hepatik yetmezliğe yol açabildiği gözlenmiştir. İzofluran ve hemodilüsyonla kombine edildiğinde alprostadil, renin-anjiotensin-aldosteron sistemi aktivasyonunda belirgin artışa sebep olmuştur. Klinik çalışmalarda izofluran anestezisinde hipotansif ajan olarak trimetafan ile karşılaştırıldığında spinal cerrahide medüller kan akımını modifiye etmediği, diz cerrahisinde venöz tonusu sürdürerek kardiyak debi artışı sağladığı ve nitrogliserinin yaptığı oksijen kullanımı ve karbondioksit eliminasyonunu modifiye etmediği bildirilmiştir. İzofluran ve sevofluran ile kombine edildiğinde alprostadil, kalça cerrahisinde kan kaybını azaltmıştır fakat kesi bölgesinde flebite sebep olmuştur.
KH’da alprostadilin kar/zarar oranı düşüktür.
Kalsiyum Kanal Antagonistleri
Kalsiyum kanal antagonistleri verapamil, diltiazem, nikardipin ve nifedipin, farklı tabiatta olsalar da, kalsium kanallarından hücre içine kalsiyum geçişini inhibe ederler. Nifedipin KH için kullanılmamıştır; verapamil ise sadece bir kez, kontrol grubu olmayan bir çalışmada kullanılmıştır. Her ajanın fizyolojik etkisi farklı olsa da hepsi vazodilatasyon, miyokard kasılma gücünde azalma ve iletimde yavaşlama sağlar. Diltiazemin negatif kronotrop ve dromotrop etkisi varken nikardipinin, düz kas liflerini gevşeterek ve özellikle sempatik sinir blokajı ile periferik vazodilatör etkisi vardır. Miyokard kasılma gücü her iki ajan tarafından azaltılsa da, sempatik sinir yanıtı, inotropizmin azalmasını engeller ve kardiak çıkımda artışa sebep olur.
Bir benzodiazepin olan diltiazem, spinal cerrahide kan kaybını azaltmak ve nitroprussidin dozunu azaltmak için başarıyla kullanılmıştır. Bir dihidropiridin olan nikardipinin köpeklerde sistemik, koroner ve serebral damarlarda vazodilatör etkisi, miyokard kasılması ve pulmoner sirkulasyonda küçük yararları vardır. Diltiazem ve nikardipin kombinasyonu KH esnasında kalp atımındaki düşük frekanslı sempatik indüksiyonlu varyasyonları, sadece nikardipinden daha fazla modifiye etmez. Nikardipin, nitrogliserin ve alprostadilin aksine, propofol ve fentanil anestezisinde serebral mikrovasküler otoregülasyonda düşüşe sebep olmuştur. Esas olarak ortopedik cerrahide kullanılmıştır, bazen uzayan hipotansiyon sonucunda kan kaybını azaltır, böylece plasma renin aktivitesi ve katekolamin seviyesindeki artışa rağmen rebound hipertansiyona sebep olmaz. Spinal cerrahide nikardipin, izofluran kadar kan kaybını azaltırken, vertebral kas kan akımını arttırmıştır. İzofluran ve sufentanil ile birlikte nikardipinin yararı ve etkinliği, pediatrik cerrahide de belirtilmiştir.
Fenoldopam
Direkt vazodilatör olan fenoldopam, renal, koroner, serebral, muskuloskeletal ve dalak sirkulasyonuna etki eden selektif periferik dopamin DA1 reseptör agonistidir. Fenoldopam arteryel vazodilatasyon yapar ve kan basıncını azaltır. Nitroprusside kıyasla, renal kan akımını arttırmış ve rebound hipertansiyon yapmadan diürez sağlamıştır. Ciddi hipertansiyonda, çocuklarda ve kardiyak cerrahide koroner revaskülarizasyonu bozmadan veya koroner spazm yapmadan kullanılmıştır; fakat intraoküler basıncı arttırmıştır. Köpeklerde hipotansiyon esnasında renal kan akımını ve glomerüler filtrasyonu sürdürdüğü gösterilmiştir; fenilefrinin basınç restorasyonuna rağmen serebral kan akımını azalttığı görülmüştür. Çocuklarda yapılan retrospektif bir çalışmada, fenoldopam KH’da etkili olmuş ve iyi tolere edilmiştir. Fenoldopamın etkinliği ve yan etkileri hakkında ileri araştırmaya ihtiyaç vardır.
Otonom Sinir Sistemi İnhibitörleri
Trimetafan kamsilat: Trimetafan, sempatik ganglionlarda sinaptik iletiyi bloke eder, böylece hormonal sempatik tepki veya plazma renin aktivitesinde modifikasyon olmadan, ilaç sonrası rebound hipertansiyon gelişmeksizin arteryel ve venöz vazodilatasyon yapar, miyokard kasılmasını ve kardiyak debiyi azaltır. Bununla birlikte parasempatik blok devam edebilir ve taşikardi, midriazis ve üriner retansiyona yol açabilir. Midriazis, silier ganglion blokajına bağlıdır ve serebral iskemi riski yaratabilir. Tartışılan diğer ajanlarla kıyasla, trimetafan serebral damarlarda vazodilatasyon oluşturmaz, kafa içi basınca minimal etkisi vardır ve serebral kan akımı otoregülasyonuna uyar. Fakat spinal cerrahide medüller kan akımı trimetafan ile, alprostadilden daha fazla etkilenmiştir. Sıçanlardaki bir çalışmada çok düşük OKB’da (30mm Hg) bile serebral kan akımı nitroprussidde doğru değerde kalırken trimetafanda azalmıştır. Trimetafan, plazma kolinesterazları tarafından metabolize edilir, çok kısa yarılanma ömrü vardır ve böbrekten atılır. Histamin salınımı ve bronşial spazmın da eşlik ettiği taşiflaksiye sebep olabilir. Trimetafan, plazma kolinesterazını inhibe ederek kürar etkisini uzatır. Bu dezavantajları, özellikle kendini gösterdiği beyin cerrahisinde kullanımını azaltmıştır.
Klonidin
Santral alfa-2 adrenoseptör agonisti olan klonidin, sempatik sinir impulslarını azaltır; dolayısıyla bradikardi ve hipotansiyona sebep olur ki bu da KH için diğer ajanlara ek olarak kullanılmasına olanak sağlar (izofluran,labetalol,urapidil). Klonidin, bu diğer ajanların hipotansif etkisini arttırıp yan etkilerini (taşikardi, toksisite, rebound hipertansiyon) azaltarak konsantrasyonlarının düşürülmesine olanak sağlar. Etkisinin öngörülememesi nedeniyle sadece oral premedikasyon olarak başarıyla kullanılmıştır. Alprostadil ile kombine edildiğinde KH için gerekli olan alprostadil seviyesini düşürür ve kan kaybında belirgin azalma sağlar.
Urapidil ve Fentolamin
Bu ajanlar periferik alfa-2 adrenoseptörler aracılığıyla vazodilatasyon oluşturur. Ek olarak urapidil kranyal sinir sisteminde serotonin reseptörleriyle etkileşir ki bu da sempatik sinir sistem yanıtının yokluğunu açıklar. Bu ajanlar serebral dolaşıma çok az etkilidir. Yine de bu ajanlar KH için yeterince düşük seviyelerde kan basınçları oluşturmamaktadır ve bu endikasyon için daha ileri çalışmalar yapılmamıştır.
Labetolol
7:1 oranında beta-1 ve beta-2 adrenoseptör ve alfa-1 adrenoseptör yarışmalı antagonistidir. Miyokard kontraktilitesini ve kalp hızını beta adrenoseptör üzerinden azaltır ve alfa antagonist etkisiyle de vazodilatasyona sebep olur. Etkinin başlama süresi yavaştır (5-10 dak); 1-3 saat arası pik etkisi vardır. İstenmeyen etkileri kullanılan anestezi tekniğine bağlıdır. İsofluranla sinerjisi optimal düzeydedir. Labetolol intrakranyal basıncı değiştirmez fakat intrakardiyak iletim bloğu, bronşiyal spazm, kalp yetmezliği, uzamış hipotansiyon riski gibi beta adrenoseptör antagonistlerinin tüm yan etkilerine sahiptir. Bunlar KH için kullanımını sınırlandırılmıştır.
Esmolol
Kısa etkili kardiyak beta-1 antagonistidir. Etkinin başlama süresi yaklaşık 3 dak, etki süresi 10 dakikadır. Eritrosit esterazlarla hidrolize edilir ve eliminasyonu hepatik, renal fonksiyonlardan bağımsızdır. Tek başına veya diğer ajanlarla birlikte kullanılabilir. Plasma renin aktivitesinde ve katekolamin seviyelerinde düşürerek kalp atım hızını ve kalp debisini düşürür ve bu yolla kan basıncını indirir. Periferik vasküler rezistanstaki artış miyokardiyal kontraktilitede azalmaya yol açar; kalp yetmezliği riski nedeniyle dikkatli kullanılmalıdır. Orta kulak cerrahisinde mikrodolaşımın otoregülasyonunu bozmadan cerrahi görüş kalitesini arttırdığı bildirilmiştir.
Diğer KH teknikleriyle karşılaştırıldığında kar/zarar oranı iyi değildir.
ACE (angiotensin-converting enzyme) İnhibitörleri
ACE inhibitörlerinden sadece kaptopril ve enalapril KH’da yardımcı olarak kullanılmıştır. Uzun etki süresi, etki başlangıç süresinin ve eliminasyonun uzun olması istenmeyen etkileri olarak görüşülür.
ACE inhibitörlerinin hipotansif etkisi anjiotensin 2’nin direkt vasokonstriktör etkisini inhibe etmesinin sonucudur. oral premedikasyonda kaptopril ve enalaprilin rolü vazodilatörlerle ortaya çıkan sempatik sinir sistemi cevabının ortadan kaldırması ve ihtiyaç duyulan nitroprussid miktarını azaltmasıdır. Kaptopril kullanımındaki tehlike renal arter stenozunda efferent küçük arterlerin vazodilatasyonundan dolayı renal yetmezlik ve onu takip eden glomerüler filtrasyon basıncında düşüş riskidir. Kaptoprilin fentanil ve propofolle kombinasyonu, nitroprussidle karşılaştırıldığında endoskopik sinus cerrahisindeki cerrahi görüş kalitesini arttırmıştır.
Operasyonlara Göre KH Teknikleri
KBB: Orta kulak cerrahisinde mikroskop ile görüşü arttırmak için sahanın kansız olması gereklidir. KH yüksek zorluk derecesi ve afferent damarları klempleyerek kanamayı durdurmadaki imkansızlık nedeniyle endikedir (vertebral baziller arter ve eksternal karotis arteri). Bu özellik endoskopik sinüs cerrahisinde daha da belirgindir.
Randomize kontrollü çalışmalar, kanamayı azaltmada ve cerrahi saha kalitesini arttırmada bazı KH tekniklerinin yararını göstermiştir. Farmakolojik ölçümler başın 15-20º kaldırılması gibi fiziksel özelliklerle de ilişkilidir. Kronolojik olarak nitroprussid, propranolol, esmolol, labetolol, nitrogliserin, alprostadil, klonidin, urapidil, kaptopril ve remifentanil, başarıyla kullanılmıştır.
Pediatrik Spinal Cerrahi: Halotan, izofluran ve sevofluran ile KH sağlanmış ve yalnız kullanıldığında da, nikardipin, nitroprussid veya fenoldopamla kombine edildiğinde de iyi sonuçlar elde etmiştir. Çocuklarda sevofluran (%2) ile beraber remifentanil, orta kulak cerrahisinde tatminkar cerrahi koşullar sağlamıştır.
Diğer Cerrahiler: Ortopedik cerrahi, oromaksillofasial cerrahi, ürolojik cerrahi ve beyin cerrahisi için KH tekniklerinde ilaçların spesifik kullanımı konusundaki çalışmalar bulunmaktadır.
SONUÇ
KH’un kanamayı azaltma ve kan tasarrufu açısından hala önemli bir rolü vardır. Kansız ameliyat sahası gerektiren cerrahilerde, mikrocerrahi (orta kulak) gibi düşük veya orta hemorajik potansiyelde, oftalmolojik cerrahide ve beyin cerrahisinde, kar zarar oranı ışığında endikedir.
Yeni inhalan ajanların (izofluran, desfluran ve sevofluran) veya kolay kontrol edilen yeni opioid remifentanile eklenen total intravenöz propofol anestezisinin hipotansif etkileri, spesifik güçlü hipotansif ajanların kullanımını ortadan kaldırıp kar/zarar oranını arttırmıştır. Standart klinik konsantrasyonlarda uygulanan bu hipotansif anestezi metodu, arteryel kateterizasyon olmadan da kullanılabilir.
Güncel tıbbi literatürde bu alanda çalışmaların bulunmaması göstermiştir ki, kardiyak cerrahi veya karaciğer transplantasyonu gibi yüksek hemorajik potansiyelli cerrahilerde KH’un kullanımı azalmış veya kaybolmuştur. Perfüzyon basıncının bazal seviyelere yakın sürdürülme ihtiyacı, antifibrinolitiklerin katkısı ve programlı otolog transfüzyon metodları, bu alanlarda KH’un kullanılmamasını açıklayabilir.
Vasküler cerrahi, kalça, diz veya spinal protez cerrahisi, mandibuler osteotomi veya prostatektomi gibi orta düzey hemorajik potansiyelli ameliyatlar, hemodilüsyon ve otolog transfüzyonun ve KH’un kombinasyonundan faydalanır.
En fazla yarar, kullanım kolaylığı ve toksisite yokluğu, klinik konsantrasyonlardaki analjezi ve hipotansiyonu birleştiren hipotansif anestezi tekniklerine aittir. İlk ve en eski seçenek epidural anestezidir, fakat bu her zaman bütün cerrahilerde pratik değildir. En son tatminkar teknik, klinik konsantrasyonlarda remifentanil ve propofol veya inhalan ajan (izofluran, desfluran veya sevofluran) kombinasyonudur. Son literatür ışığında ve güvenlik ve kullanım kolaylığı nedeniyle, her iki teknik de tercih edilebilir.
Fadel Hawas