Güncel Anestezinin son iki bölümü pediatrik hastalarda peroperatif sıvı idamesi ve replasmanı üzerineydi. Kafalar berraklaşacağına daha çok karıştı sanırım. Konu henüz netlik kazanmış değil. Laktat metabolizması ve karaciğer fonksiyonları dikkate alındığında pediatrik grupta ringer laktat problem yaratabilir mi diye bir sürü literatür karıştırdım. Çocukta sıvı resüsitasyonunda kristalloid seçilecekse salin ve ringer laktat öneriliyor (British Journal of Anaesthesia, CEPD Reviews, Volume 3 Number 1, 2003).
Erişkinde ringer laktatın içeriğinin fizyolojik elektrolit düzeylerine daha yakın olduğu ve büyük miktarlarda sıvı resüsitasyonunda hiperkloremik asidoza yol açan saline oranla üstünlüğü ve ilk seçenek olması gerektiği bildirilmiş (Continuing Education in Anaesthesia, Critical Care & Pain, Volume 4, Number 4, 2004). Öte yandan hemorajik şokta çok miktarda eksojen laktat (ringer laktat solüsyonu) kullanılarak resüsite edilen erişkinlerde kan laktat düzeyinin şoka bağlı laktat artışından daha fazla olduğu da bildirilmiş (Anasthesiol Intensivmed Notfallmed Schmerzther 2002, 37:356). Gelecekte laktatsız solüsyonların daha yaygın kullanılacağı düşünülüyor.
Travma hastalarında hastaneye girişte bakılan laktatın sürvi için prognostik olduğu çok sayıda çalışma ile belirlenmiş. Sıvı resüsitasyonu için kullanılan ringer laktat bu değeri etkileyip yanıltıcı olabilir mi deniyor (Critical Care 2005, 9:441-453).
Günlük laktat döngüsü 1300 mmol/24 saat olabiliyor. Laktat karaciğerde glukoneogeneze girip metabolize ediliyor, hidrojen iyonları kullanılıyor, bikarbonat ise asidozu düzeltmede işe yarayabiliyor. Kritik hastada bu metabolik yol bozulursa veya artan bikarbonatın renal atılımı etkilenirse (kritik hastaların bir kısmı zorunlu asidik idrar üretiyor) alkaloz ve hipokalemi gelişebiliyor. Diabetes mellitusta ise şeker kontrolü kötü vakalarda laktatın glukoza dönüşümü ile glukoz düzeyi artacağından ringer laktattan kaçınılması gerekiyor (Continuing Education in Anaesthesia, Critical Care & Pain, Volume 5, Number 5, 2005).
Laktatın hepatik metabolizması 100 mmol /saat; akut renal yetersizlikte ise bu 0.6 mmol/kg/saat’e düşebiliyor (Intensive Care Med 1999; 25: 1209). Ringer laktatta 29 mmol/L olduğu düşünülürse hemodinamisi iyi normal hastada peroperatif replasmanda kullanımı sorun yaratmayacaktır. Ciddi karaciğer hastalığında metabolik hızı düşeceğinden ringer laktat seçilecek sıvı olmamalı. Öte yandan karaciğer transplantasyonunda özellikle anhepatik fazda laktatın böbrek fonksiyonları iyi hastada beklendiği oranda artmadığı biliniyor ve bu da renal laktat metabolizmasına bağlanıyor.
Bu uzun girişten sonra gelelim yeni konumuza:
Plazma laktat konsantrasyonunun normal değeri 0.3-1.3 mmol/L ve laktat üretimi ile laktat metabolizması arasındaki dengeyi ifade ediyor. İnsanda laktat L-isomeri halinde bulunuyor.
Normal Laktat Üretimi
Laktat üretiminin kaynağı eritrositler, perivenöz hepatositler, iskelet kası miyositleri ve cilt. Bazal üretilen miktar ise 0.8 mmol/kg/saat (1300 mmol/gün).
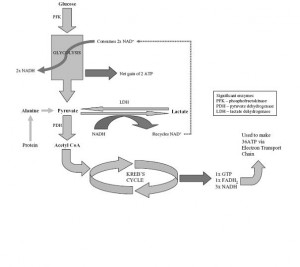 Figür 1‘de (solda) glikoliz ve laktat üretimi görülmekte.
Figür 1‘de (solda) glikoliz ve laktat üretimi görülmekte.İki yöntem kullanılıyor: Spektrofotometrik yöntemle proteinden arınmış kanda ölçüm veya kan gazı analizörlerinde ölçüm. İkinci yöntem laktatı %13 kadar yüksek ölçüyor, ancak sonuç hematokrite göre düzeltilirse bu fark azalıyor. In vitro eritrosit glikolizi devam ettiğinden tam kanda ölçülen laktat yanlış yüksek çıkıyor; dolayısı ile hemen ölçüm yapılmayacaksa kanın soğutularak veya proteinleri presipite ettirilerek ya da glikoliz inhibitörleri eklenerek stabilize edilmesi şart.
Laktat ve Laktik Asidoz
Laktik asitten dissosiye olan H+ iyonları oksidatif fosforilasyon ile ATP üretiminde kullanılabilmekte. Laktat üretimi devam ederken oksidatif yolda bozukluk olursa H+ iyonları artıp asidoza yol açıyor. Ağır egzersiz sırasında oksidatif fosforilasyonun devam etmesi ciddi boyuttaki laktat üretimine rağmen asidoz gelişmesini engelliyor.
NADH ve NAD+
Glikoliz NAD+ (nikotinamid adenin dinukleotid) üretimini gerektirir. NADH sunumu piruvatın laktata dönüşüm hızını denetler. Kalp gibi çok miktarda ATP gerektiren dokuların piruvatın asetil CoA’ya dönüşümüne gereksinimi vardır. NADH düzeyini düşük tutmak için mitokondrial membranda elektronların taşınmasına yardım edecek ve NADH’yı NAD+ haline okside edecek taşıyıcılar kullanılır. Malat-aspartat yolu temel taşıyıcı mekanizmadır. Gliserol-fosfat taşıyıcı yolu ise sekonder role sahiptir. Bu ikisi oks-fos taşıyıcı olarak bilinir.
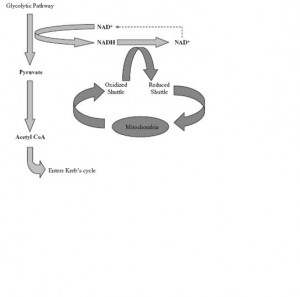 Figür 2‘de (solda) oks-fos taşıyıcı sistemi görülmekte.
Figür 2‘de (solda) oks-fos taşıyıcı sistemi görülmekte.
Glikoliz hızı oks-fos taşıyıcı sisteminin kapasitesini aşacak ölçüde artarsa NADH konsantrasyonu artar ve laktat üretimi ile NAD+’yı rejenere eder; sonuçta laktat konsantrasyonu yükselir.
Karaciğer laktatın %70’ini temizler. Karaciğerin laktatı alması hem bir monokarboksilat taşıyıcısı hem de daha az olarak difüzyonla olur (>2 mmol/L düzeyindeki konsantrasyonlarda önemli). Periportal hepatositlerde laktat glukoneogenez ve daha az olarak da CO2 ve suya oksidasyon şeklinde metabolize edilir. İskelet ve kalp kası miyositleri gibi mitokondriden zengin dokular ve proksimal tubulus hücreleri laktatın kalanını piruvata dönüştürerek uzaklaştırır. Bu işlem için oks-fos taşıyıcı sisteminin sağladığı NAD+ gereklidir. Laktatın %5’den azı ise renal yolla atılır.
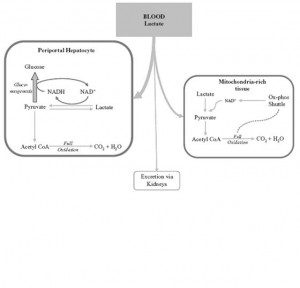 Figür 3‘de (solda) laktatın plazmadan uzaklaştırılması şematik olarak izlenmekte.
Figür 3‘de (solda) laktatın plazmadan uzaklaştırılması şematik olarak izlenmekte.1. Laktat Üretiminde Artış
Hiperlaktatemi (> 5 mmol/L) Tip A (doku hipoksisi tüketimden fazla laktat üretimine neden olur) ve Tip B (doku hipoksisinin rolü yok) olarak olarak ikiye ayrılmaktadır. Tip B’nin de nedene göre 3 tipi vardır: B1 (altta yatan hastalığa bağlı), B2 (ilaç ve toksinler), B3 (doğumsal metabolizma bozuklukları). Ancak bu klasifikasyon olayı basite indirgemektedir, oysa kritik hastadaki problem genellikle multifaktöryeldir.
Artmış glikoliz: Glikoliz artışının sağlanabilmesi için piruvatın laktata dönüşümünde ortaya çıkan NAD+’a gerek vardır. Fosfofruktokinaz (PFK) aktivitesi hız sınırlıdır. Hipoksemi, anemi, hipoperfüzyon, ağır egzersiz ve karbon monoksit intoksikasyonu gibi durumlarda ATP miktarının azalması, AMP miktarı artışına paralel olarak PFK’ı stimüle eder. Ayrıca endojen ve eksojen katekolaminler de glikolizi stimüle eder.
Ağır egzersizde tip II miyositler büyük miktarda laktat üretir (konsantrasyon 25 mmol/L’ye ulaşabilir, soruna yol açmaz). Bu artan kardiyak enerji gereksiniminin bir miktarını karşılar. Ağır egzersizi takiben gevşeme döneminde tip I kas lifleri artmış laktat metabolizmasından sorumludur.
Metabolizma bozuklukları: Doğumsal metabolik bozukluklar, tiamin eksikliği ve endotoksin varlığında piruvat dehidrogenaz aktivitesi bozulur. Kritik hastalık veya malignitede oluşan protein katabolizması alanin üretir ve bu da piruvata dönüşür. Krebs siklüsünün veya elektron transport zincirinin herhangi bir defekti piruvat birikimine neden olur.
2. Hepatik Laktat Klerensinin Azalması
Karaciğer kalp debisinin %25’ini alır. Portal ven hepatik kan akımının %75’ini, oksijenin %50-60’ını sağlar. Hepatik kan akımında veya oksijenasyonunda değişme veya intrensek karaciğer hastalığı karaciğerin laktatı metabolize etme kapasitesini etkiler.
Karaciğer kan akımı normalin %25’ine düşerse laktat klerensi azalır. Ağır şokta monokarboksilat taşıyıcısı tarafından laktat alımı satüre hale gelir, intrasellüler asidoz gelişiminde glukoneogenez inhibe olur ve azalmış karaciğer kan akımı metabolize edilmek üzere daha az laktat taşır. Anaerobik şartlarda hepatik enerji üretiminin temel biçimi glikolizdir. Böylece karaciğer laktatı glukoneogenez için kullanan organ yerine laktat üreten organ haline gelir.
Oral hipoglisemik ilaçlar: Laktatı piruvata dönüştürmek için gerekli NAD+’yı glukoneogenez sağlar. Biguanid oral hipoglisemik ilaçlar hepatik ve renal glukoneogenezi inhibe eder (metformin sadece renal yetersizlikte laktat metabolizmasını etkiliyor gibi görünmektedir). Metformin renal ve hepatik yetersizlikte kontrendikedir. NAD+ sunumu alkol dehidrojenaz gibi diğer enzim sistemlerinin tüketimine hassastır (etanol intoksikasyonunda bu enzimin aktiflenmesi ile belirgin hale gelir). Tip I diabette glukoneogenez bozulur.
Hartmann solüsyonu: Bu solüsyonun güçlü iyon farkı (SID) 28 mEq/L’dir. SID değerinin 0 olduğu %0.9 NaCl solüsyonuna göre normal değer olan 40-42 mEq/L’ye daha yakındır. Bu nedenle %0.9 NaCl’e göre daha az hiperkloremik asidoza yol açar. Laktat (29 mmol/L) güçlü iyon olarak etki gösterdiğinden karaciğer tarafından metabolize edilene dek geçici olarak asidoza yol açar.
3. Sepsis
Her ne kadar endotoksine veya travmaya cevap olarak fagositik hücrelerde aşırı laktat üretimi hiperlaktatemiye neden olsa da, hepatik laktat ekstraksiyonu ve utilizasyonundaki azalma da olaya katkıda bulunmaktadır.
4. Kronik Hastalık
Kronik hastalıklı karaciğerin laktatı işleme yeteneğindeki azalma periferik üretim arttığında veya karaciğerde daha fazla hasar oluştuğunda belirgin hale gelir.
5. Ekstrahepatik Metabolizmanın Azalması
Oksijen sunumunda azalma veya oksidatif yollarda intrensek bir problem olduğunda mitokondriden zengin dokuların laktatı metabolize etmesi azalacaktır. Bu durumda laktat tüketen değil üreten organlar haline geleceklerdir.
6. Renal Atılımın Azalması
Böbrekler laktatı ekskresyon, glukoneogenez ve oksidasyon biçiminde işlerler. Renal eşik 6-10 mmol/l’dir. Renal ekskresyon sadece hiperlaktatemide önemli hale gelir.
Laktat ve Kritik Hastalık
Ciddi asidoz (pH<7.35)> 5 mmol/L olduğunda mortalite %80’dir.
1. Kardiyak Arrest ve Resüsitasyon
Kardiyak arreste veya ağır hipovolemiye bağlı hipoksi anaerobik metabolizmayı tetikler. Laktat düzeyi direkt olarak hücre hipoksisini yansıtır. Hastane içi kardiyak arrest sırasında ve spontan dolaşımın başlamasından 1 saat sonra bakılan laktat düzeyi sürvi için prediktiftir.
2. Sepsis
Sistemik inflamatuar cevap sendromunda (SIRS) veya erken sepsiste hiperlaktatemi doku hipoksisini yansıtabilir. Oksijen sunumunun erken dönemde arttırılabilmesi sonucu iyileştirebilir. Sepsis tablosu oturduktan sonra bakılan laktat düzeylerinin yorumlanması zordur. Stabil septik hastaların oksijen sunumu artmıştır; doku oksijen düzeyleri genellikle anaerobik metabolizmayı tetikleyen düzeyin üzerindedir. Bozulmuş laktat klerensi genellikle artmış üretimden daha önemlidir. Bu hastalarda aerobik laktat üretimi stres altında karbonhidrat metabolizmasının değişimine bağlı olabilir. Dikloroasetat piruvat dehidrogenaz aktivitesini arttırarak ve septik hastada kan laktat düzeyini düşürmektedir, ancak hemodinami veya sürvi üzerine etkisi yoktur.
3. İntestinal İnfarkt
Barsak hipoksisi anaerobik metabolizmaya yol açar. Karaciğere portal ven üzerinden daha fazla laktat ulaşır. Başlangıçta peripotal hepatositler laktatı okside eder veya glukoza çevirir. Bakteriyel translokasyon ve ciddi sıvı kaçağı dolaşım kollapsına katkıda bulunur. Global olarak oksijen sunumu azalır. Endojen katekolamin salgılanması dolaşımı ayakta tutmaya çalışır, ama aynı zamanda glikoliz ve laktat oluşumunu da arttırır. Şok geliştiğinde hepatik kan akımı azalır intrasellüler asidoz laktattan glukoneogenez oluşumunu inhibe eder. Karaciğerde laktat klerensi yerine üretimi baskın hale gelir. İntestinal bakteriler glukozu ve karbonhidratı D-laktat’a metabolize eder. Bu ise insan LDH’ı tarafından yavaş olarak metabolize edilebildiğinden ve laktik asidoz oluşumuna katkıda bulunur.