Anestezi sırasında hastanın pek çok kimyasal ile teması oluyor. Bunlardan en sık kullanılan ilaç ve maddelerin allerjik potansiyeli, allerji oluşturma mekanizması ve tanıda yararlanılacak testler serinin bu yazısının konusu olacak.
Antibiyotikler
Tüm antibiyotikler anafilaksiye neden olabilir. En fazla penisilinlerle görülen reaksiyonların sıklığı 1/1000 uygulama olarak bildirilmektedir. Fransa ve Danimarka’da anestezi sırasında görülen anafilaktik reaksiyonların %15’i antibiyotiklere olarak bağlı rapor edilmiştir. Ancak penisilin allerjisi olduğunu söyleyen pek çok hastada, semptomların allerjik tipte olmadığı ortaya çıkmaktadır. Bu nedenle döküntü, kaşıntı veya anafilaktik şok gibi allerjik semptomların direkt olarak sorgulanması önemlidir.
Mekanizma ve çapraz reaksiyonlar: İlk uygulamada anafilaksi gelişebilir, beta-laktam antibiyotikler (aminopenisilinler, sefalosporinler, karbapenemler) ile çapraz reaksiyon görülebilir. Ancak önceki yıllarda anafilaksi insidansının olduğundan daha yüksek olarak düşünüldüğü, bu nedenle günümüzde penisilin allerjisi olan hastalarda sefalosporinlerin kullanılabileceği dikkate alınmalıdır.
Tanı: Çoğu ülkede penisilin allerjisi için testler allerji uzmanları tarafından ve IgE antikor ölçümü, cilt testleri ve provokasyon yöntemi ile uygulanmaktadır. Diğer antibiyotiklere karşı da cilt testleri uygulanmakla beraber deneyim yetersizdir. Amoxicilloyl, ampicilloyl, penicilloyl G, penicilloyl V, cefaclor, erythromycin, penisilin minor determinantları, beta-laktamlar, tetrasiklinler, sefalosporinler ve kinolonlara karşı IgE antikorları gösterilmiştir, ancak test için bunların bazıları piyasada bulunmamaktadır.
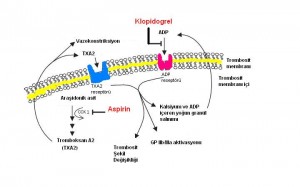
Aspirin ve non-steroid anti-inflamatuar ilaçlar (NSAID)
Genel popülasyonda allerjik reaksiyon sıklığı %1 kadardır. Ancak non-allerjik astma ve nazal polipozis olan hastalarda sıklığı daha yüksektir. Anestezi ile bağlantılı olarak bu ilaçlara karşı anafilaksi nadirdir.
Mekanizma ve çapraz reaksiyonlar: Bu ilaç grubuna karşı reaksiyonlar non-allerjiktir. Ancak pirazolonlara karşı IgE aracılıklı reaksiyon bildirilmiştir. Aspirin ile çoğu NSAID arasında çapraz reaksiyon vardır. Aspirine duyarlı hastalarda parasetamole çapraz reaksiyon ancak yüksek dozlar (>1 gr) uygulandığında görülmüştür. Aspirin/NSAID’e duyarlı hastalarda selektif COX-2 inhibitörleri güvenli olmakla beraber, deneyim yeterli değildir.
Tanı: Aspirin ve NSAID’ler IgE oluşumunu uyarmadığı için cilt testleri kullanılamamaktadır. Oral provokasyon testi tanı sağlar ve bazı merkezlerde uygulanmaktadır.
Klorheksidin
Pek çok ülkede dezenfektan olarak kullanılmaktadır. Danimarka’da anestezi sırasında görülen anafilaktik reaksiyonlarda payı %12’dir. Çoğu ülkede anafilaksi insidansı bilinmemekte ve gözden kaçtığı için de allerjen olarak şüphelenilmemektedir. Sağlık çalışanları da bu maddeyle temas etse de allerji oluşumu çok nadirdir.
Mekanizma ve çapraz reaksiyonlar: Reaksiyonlar IgE kökenlidir.
Tanı: Cilt testleri (prick test ve intradermal test) ve klorheksidine karşı IgE antikorları kullanılabilir. Anestezi, cerrahi sırasında gelişen reaksiyonlarda klorheksidin allerjisi de araştırılmalıdır.
Dekstran
Human albumin ile kıyaslandığında reaksiyon sıklık oranı 2.32’dir (1.21–4.45). Düşük molekül ağırlıklı dekstran (Promiten) ön-uygulaması sonrası ciddi anafilaktik reaksiyon sıklığı 1/70.000’dir.
Mekanizma ve çapraz reaksiyonlar: Dekstrana karşı oluşan IgG antikorları ImmunoCAP veya ELISA ile ölçülebilir. Klasik anafilaksideki IgE antikorlarının aksine IgG antikorları dekstran ile reaksiyona girdiğinde tüketilir. Çapraz reaksiyon bazı bakteriyel antijenler ile olabilir. Bu nedenle daha önce iv dekstran almamış kişilerde de allerji ortaya çıkabilir.
Tanı: Reaksiyondan sorumlu IgE olmadığından cilt testleri negatiftir. In vitro tanı yöntemleri kullanılabilir. Analizler tercihan reaksiyondan önce veya birkaç hafta sonra (reaksiyondan sonraki birkaç ay içinde) alınmış serumda yapılmalıdır. Konuda özelleşmiş merkezlerde provokasyon testleri de uygulanabilir.
Jelatinler
Diğer kolloidlere oranla anafilaktik reaksiyon riski belirgin şekilde yüksektir. Human albumin ile kıyaslandığında reaksiyon sıklık oranı 12.4’tür (6.4-24). Fransa’da yaygın olarak kullanılmakta ve anestezi sırasında görülen anafilaksilerin %4’ünü oluşturmaktadır.
Mekanizma ve çapraz reaksiyonlar: Reaksiyonlar genellikle non-allerjik olmakla beraber IgE aracılıklı reaksiyon da ortaya çıkabilir. IgE kökenlilerde neden jelatinin elde edildiği ana kaynağın (domuz, sığır) proteinlerinin kontaminasyonudur. IgE kökenli reaksiyonlarda cilt testleri ve IgE antikorları pozitif bulunabilir. Kontamine proteinlere karşı gelişen IgE antikorları için de analiz yapılabilir.
Hidroksietilnişasta (HES)
Human albumin ile kıyaslandığında reaksiyon sıklık oranı 4.51’dir (2.06-9.89). Ciddi reaksiyonlar %0.006 olarak bildirilmiştir.
Mekanizma ve çapraz reaksiyonlar: IgE antikor oluşumu nadirdir.
Tanı: Cilt testleri kullanılabilir, ama deneyim yetersizdir.
İyotlu Kontrast Maddeler
Farklı preparasyonlar vardır. Osmolaliteleri düşük veya yüksek, iyonize veya non-iyonize yapıdadırlar. Preparasyonlardaki farklı iyodin konsantrasyonu nedeniyle anafilaktik reaksiyon potansiyelleri de değişkendir. Yüksek osmolaliteli iyonik (%0.04-0.22) iyodinli kontrast maddelerde ciddi reaksiyonlar, düşük osmolaliteli non-iyonik (0.004-0.04) olanlara oranla daha sık görülmüştür. Mortalite oranı 1/170.000’dir.
Mekanizma ve çapraz reaksiyonlar: Reaksiyonların patofizyolojisi multifaktöriyeldir ve iki yolak üzerinden başlayabilir: IgE antikorlarını içeren immün yolak ve non-spesifik toksik yolak. İmmün yolak çok az miktarda antijenle tetiklenirken, non-spesifik toksik yolak ile allerjik reaksiyon gelişimi direkt olarak miktara bağlıdır.
Tanı: Cilt testleri ve provokasyon testleri kullanılabilir. Deneyim yetersizdir.
Ketamin
Anafilaktik reaksiyonları çok çok nadirdir.
Mekanizma ve çapraz reaksiyonlar: Bilgi yetersizdir. Mast hücrelerine direkt etkisi olduğu düşünülmektedir.
Tanı: Cilt testleri uygulanabilir. IgE antikorları için test bulunmamaktadır.
Doğal Kauçuk Lateks
Son üç dekadda allerji sıklığı artmıştır. Atopik yapı ve lateksle düzenli temas gerek hastalarda gerekse sağlık personelinde allerji gelişimi riskini arttırmaktadır. Anestezi sırasında latekse bağlı anafilaksi insidansı ülkelere göre değişmektedir. Fransa’da 1999-2000 yılları arasında bu sıklık %16.7 olmuştur. Danimarka’da %12, Norveç’te ise %5’in altındadır.
Mekanizma ve çapraz reaksiyonlar: Ya lateks proteinlerine karşı IgE kökenli anafilaksi veya üretimde eklenen kimyasallara karşı kontakt allerjisi egzemaya yol açar. Doğal kauçuktaki pek çok proteine karşı IgE antikorları gelişebilir ve allerjen proteine göre örneğin tropikal meyvelere, fındık ceviz gibi kabuklu yemişlere ve patatese çapraz reaksiyon görülebilir.
Tanı: IgE kökenli allerji tanısında cilt testleri, IgE antikor ölçümü, provokasyon/temas testleri kullanılabilir. Kontakt allerjisi için kauçuğa eklenen maddelerle yama testi uygulanabilir.
Lokal Anestetikler
Anafilaktik reaksiyonların insidansı bilinmemekle beraber çok düşük olduğu bildirilmektedir. İddia edilen reaksiyonların çoğunun nedeni vasovagal reaksiyonlar, aksidental damar içi uygulamaya bağlı toksik reaksiyonlar veya eklenen adrenaline bağlı semptomlardır.
Mekanizma ve çapraz reaksiyonlar: IgE aracılıklı reaksiyonlar çok nadirdir ve sıklıkları ester grubu lokal anestetiklerin kullanımının azalması ile düşmüştür. Ester grubunda çapraz reaksiyonlar sık, amid grubunda ise nadirdir.
Tanı: Çoğu tanı protokolü cilt testleri (skin prick, intradermal veya yama testi) ile başlayıp subkutan provokasyon ile devam eden bir sıra izlemektedir. Önemli olan şüpheli lokal anestetiği test ederken uygun bir alternatifin de test edilmesidir. Henüz kullanımda olan lokal anestetikler için IgE ölçümü bulunmamaktadır.
Midazolam
Anafilaksi insidansı çok çok düşüktür.
Mekanizma ve çapraz reaksiyonlar: Mast hücrelerine direkt etki tanımlanmıştır. İmidazol halkası immün sistemin potansiyel tetikleyicisi olarak rol oynayabilir. Çapraz reaksiyon ile ilgili güvenilir veri yoktur.
Tanı: IgE antikorları için test bulunmamaktadır. Cilt testleri kullanılabilir, ancak deneyim sınırlıdır.
Nöromusküler Blokerler
Anafilaksi sıklığı ülkelere göre değişmektedir. Fransa, Norveç ve İngiltere’de yüksek (1/5.000-1/10.000), diğer ülkelerde düşüktür (1/50.000-1/150.000).
Mekanizma ve çapraz reaksiyonlar: IgE aracılıklı allerji oluşmaktadır. Epitopun (allerjende antikorun yapıştığı kısım) katerner amonyum iyonu olduğu belirlenmiştir. Bu kısım tüm nöromusküler blokerlerde, morfin, folkodin ve diğer morfin/kodein analoglarında bulunmaktadır. Nöromusküler blokerler arasında çapraz reaksiyon sıktır (>%70).
Tanı: Cilt testi yüksek sensitivite ve spesifite nedeniyle altın standarttır. Yüksek ilaç konsantrasyonları uygulandığında yalancı pozitif sonuçlar görülebildiğinden intradermal test uygulanacaksa çok dikkat edilmelidir. Suksametonyum için IgE antikor ölçümü yapılabilir, ancak diğer ajanlar için bu test ticari olarak bulunmamaktadır. Alternatif olarak lökosit histamin salınım testi ve bazofil stimülasyon testi gibi in vitro provokasyon testleri kullanılabilir.
Opioidler
Anafilaksi insidansları düşüktür.
Mekanizma ve çapraz reaksiyonlar: Reaksiyon muhtemelen mast hücrelerine direkt etkiye bağlıdır. Morfin, kodein ve meperidin ciltteki mast hücrelerini stimüle eder. Fentanil, alfentanil ve sufentanilin mast hücrelerine lokal etkisi yoktur. Morfinde bir katerner amonyum iyonu vardır, ek olarak katerner amonyumla çapraz reaksiyonu olmayan bir başka allerjik etken de tanımlanmıştır. Morfin, meperidin, kodein ve metadon arasında çapraz reaksiyon oluşur, fentanilde ise bu belirsizdir.
Tanı: Bazı opioidlere karşı IgE antikorları belirlenmiştir, ancak allerjen epitop açısından genellikle monovalan olduklarından IgE kökenli reaksiyon oluşturmamaktadırlar.
Propofol
Anafilaktik reaksiyon nadirdir. Fransa’dan bir çalışmada oran %2.3 olarak bildirilmiştir.
Mekanizma ve çapraz reaksiyonlar: Reaksiyon muhtemelen IgE kökenli değil mast hücrelerine direkt etki ile ortaya çıkmaktadır. Propofol bir lipid taşıyıcıda çözünmektedir (soya fasulyesi, yumurta lesitini, gliserol) ve taşıyıcı proteinden arındırılmaktadır. Üreticiye göre emülsiyona karşı spesifik bir reaksiyona dair kanıt yoktur.
Tanı: Bazı uzmanlar cilt testlerini savunmaktadır. IgE testi bulunmamaktadır.
Tiopental
Anafilaksi riski 1/23.000-1/29.000 uygulama olarak tahmin edilmektedir. Daha önce ilaçla temas ve kadın cinsiyet (kadın:erkek oranı 3:1) risk faktörü olarak kabul edilmektedir.
Mekanizma ve çapraz reaksiyonlar: Reaksiyon non-allerjik, muhtemelen mast hücrelerinin direkt uyarılması ile oluşmaktadır. Ancak tiopentale karşı IgE antikorları da bildirilmiştir.
Tanı: IgE antikor ölçümü için reagent bulunmaktadır. Cilt testleri kullanılabilir.